��Ŀ����
����Ŀ������������������ʳ�ν϶��ʹ���˵����(KIO3)��������ڹ�ҵ�Ͽ��õ�ⷨ��ȡ����ʯī�Ͳ����Ϊ�缫����KI��ҺΪ���Һ����һ�������µ�⣬��Ӧ����ʽΪ��KI+3H2O![]() KIO3+3H2���������й�˵����ȷ����( )
KIO3+3H2���������й�˵����ȷ����( )
A. ���ʱ��ʯī������������������� B. ���ʱ������Ӧ�ǣ�I����6e��+3H2O=IO3��+6H+
C. ��Һ������ǿ���ԣ����������� D. ������Һ��pH����
���𰸡�B
��������
����A.�ɵ�ⷽ��ʽ��֪���ڷ�Ӧ��I-ʧȥ���ӱ�ΪIO3-����˵��ʱ��ʯī���������������������A����;B�����ܷ�Ӧ����ʽ��֪�����ʱ��������Ӧ�ǣ�I��-6e �C+ 3H2O = IO3��+ 6H+,B��ȷ;C����Һ������ǿ���ԣ����벻��ֵ缫��Ӧ��������������C����D.��ⷴӦ����ʽΪ��KI + 3H2O![]() KIO3 + 3H2������Ӧ��������ˮ����KI��ǿ��ǿ���Σ���Һʼ�ճ����ԣ�PH=7��D����ѡB��
KIO3 + 3H2������Ӧ��������ˮ����KI��ǿ��ǿ���Σ���Һʼ�ճ����ԣ�PH=7��D����ѡB��

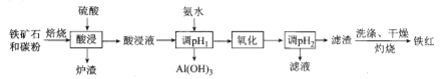
����Ŀ��ij��������Ҫ�����ᡢFe3+��Fe2+��TiO2+��Al3+ �����ø÷�Һ�Ʊ����������[( NH4) 2S2O8]��TiO2��һ�ֹ�����������:

��֪��i.TiOSO4����ˮ����ˮ������H2TiO3,��������γ��������������pH��Χ�� �±�:
�������� | TiO2+ | Fe3+ | Fe2+ | Al3+ |
��ʼ������pH | 1.2 | 1.9 | 7.0 | 3.2 |
������ȫ��pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii. pH>7 ʱ,Fe2+�������� Fe( ��)������Fe(NH3)2]2+o
��ش���������:
(1)��������Fe��������________________ .
(2)����TiO(OH)2�Ļ�ѧ����ʽΪ_______________ ��
(3)����I������II�����е����ʵĻ�ѧʽΪ_____________ .
(4)����H2O2��Ŀ���dz���Fe( ��)��������[Fe(NH3)2]2+,�˹������������뻹ԭ�������ʵ���֮�������ϵ���________ (����ֵ)��
(5)�����£���������Ҫ������ʽ��pH�Ĺ�ϵ����ͼ��ʾ��

��Pt�缫��ⱥ��NH4HSO4��Һ�Ʊ����������ʱ��Ϊ�����������ŵ��������ҪΪ HSO4-��Ӧ������������Һ��pH��Χ��______֮��,��缫��ӦʽΪ____________ ��
(6)������Ա�����������[NH4Fe(SO4)2]�ζ����ⶨTiO2�Ĵ��ȣ��䲽��Ϊ�� ���������ܽ�wg ����������Ʒ������������ԭ�������ˡ�ϴ�ӣ�����Һ����Ϊ100 mL,ȡ 25.00 mL,��NH4SCN��ָʾ�����ñ����������Һ�ζ����յ㣬��Ӧԭ��Ϊ: Ti3++Fe3+=Ti4++Fe2+��
���жϵζ��յ�ķ�����________________________ ��
�ڵζ��յ�ʱ����c mol/L-1 NH4Fe(SO4)2��ҺVmL,��TiO2����Ϊ___________(д�������ĸ��ʾ�Ĵ���ʽ)��
����Ŀ����֪��2CH3OH(g)![]() CH3OCH3(g)��H2O(g)����H����25 kJ/mol��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�
CH3OCH3(g)��H2O(g)����H����25 kJ/mol��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
c/(mol��L��1) | 0.8 | 1.24 | 1.24 |
����˵����ȷ����(����)
��ƽ��������¶ȣ�ƽ�ⳣ��>400
��ƽ��ʱ��c(CH3OCH3)��1.6 mol/L
��ƽ��ʱ����Ӧ��������������С20 kJ
��ƽ��ʱ���ټ�������ʼ������CH3OH������ƽ���CH3OHת��������
�ݴ�ʱ�̷�Ӧ�ﵽƽ��״̬
��ƽ��ʱCH3OH��Ũ��Ϊ0.08 mol��L��1
A. �٢ڢܢ� B. �ڢ� C. �ڢۢܢ� D. �ڢܢ�