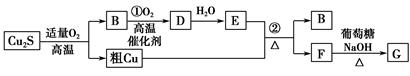
题目内容
现有含Fe(NO3)3、Cu(NO3)2、HNO3的某稀溶液,若向其中逐步加入铁粉,溶液中Fe2+浓度与加入铁粉的物质的量之间的关系如图所示,则该溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为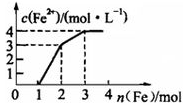
| A.1∶1∶3 | B.1∶2∶4 | C.1∶1∶4 | D.1∶3∶1 |
C
解析试题分析:由图可知,加入铁粉后反应先后顺序是:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O、Fe+2Fe(NO3)3=3Fe(NO3)2、Fe+Cu(NO3)2=Fe(NO3)2+Cu;设HNO3、Fe(NO3)3、Cu(NO3)2分别为xmol、ymol、zmol,由于先加入1molFe时没有生成Fe2+,只生成1mol Fe(NO3)3,由系数之比等于物质的量之比可得:n(HNO3)=4n(Fe),则x=4;再加入1molFe时生成3molFe2+,说明参加反应的Fe(NO3)3为2mol,则y=1;最后加入1molFe时生成1mol Fe2+,说明z=1;因此,该溶液中Fe(NO3)3、Cu(NO3)2、HNO3分别为1mol、1mol、4mol,三者的浓度之比为1∶1∶4,故C正确。
考点:本题以铁及其化合物的重要性质为线索,以图像为载体,主要考查氧化还原反应的先后顺序、物质的量在化学方程式计算中的应用、物质的量浓度的计算等基础知识和基本技能。

下列反应中氯元素被氧化的是( )
A.MnO2+4HCl MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ |
| B.2HCl+Ca(OH)2=CaCl2+2H2O |
| C.5Cl2+I2+6H2O=10HCl+2HIO3 |
D.2KClO3 2KCl+3O2↑ 2KCl+3O2↑ |
铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)可氧化硫酸锰(MnSO4),反应的离子方程式为5NaBiO3+2Mn2++14H+=2MnO- 4+5Bi3++Na++7H2O,下列说法错误的是
| A.若有0.1mol氧化产物生成,则转移0.5mol电子 |
| B.铋酸钠难溶于水 |
| C.该反应可以用于鉴定Mn2+离子 |
| D.该反应可以用浓盐酸酸化 |
在熔融KOH中大气中的氧可将铬铁矿FeCr2O4中Fe和Cr的化合价都转化为+6价,氧化 1 mol FeCr2O4在理论上需要多少摩尔氧气
| A.2mol | B.2.5mol | C.3mol | D.4mol |
已知5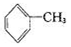 +6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+_______。
+6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+_______。
下列说法不正确的是
A.氧化产物为 | B. 作氧化剂 作氧化剂 |
| C.每1mol KMnO4转移5mol e- | D.H2SO4起酸的作用 |
将1.95g锌粉加入到200mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是( )
| A.M | B.M2+ | C.M3+ | D.MO2+ |
已知Br2+ 2Fe2+ = 2Fe3++ 2 Br-,当向含1 molFeBr2溶液中逐渐通入Cl2,溶液中有一半的Br-氧化时,下列判断不正确的是
| A.反应前后溶液的颜色发生了改变 |
| B.反应后溶液中c(Cl-)= C(Br-) |
| C.参加反应的Cl2为1 mol |
| D.反应的离子方程式为:2Fe2++ 2Br- + 2Cl2= 2Fe3++ Br2 + 4Cl- |