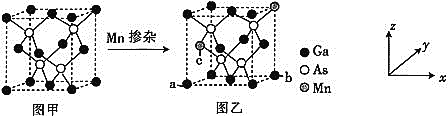
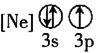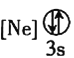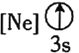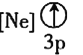��Ŀ����
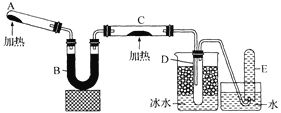
����Ŀ����֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ������ͼ�е�װ�ã�ʡ�Լг�װ�ü�����װ�ã�����ʵ�ָ÷�Ӧ��ʵ��ʱC�з�ĩ��Ϊ��ɫ��D�г�����ɫҺ�塣�����й�˵����ȷ���� ( )
A.�Թ�A�м�����Լ�ΪNH4Cl����
B.��Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ2 : 3
C.װ��B�м�������ʿ����Ǽ�ʯ�һ���ˮ�Ȼ���
D.װ��D��Һ�����ʹ����ĺ�ɫʯ����ֽ����
���𰸡�D
��������
��ͼ��֪��A�з���![]() ��BΪ���ﰱ����C�з���
��BΪ���ﰱ����C�з���![]() ��D����ȴ����Һ��Ϊˮ�Ͱ�������E���ռ�������
��D����ȴ����Һ��Ϊˮ�Ͱ�������E���ռ�������
A.ʵ������ȡ����Ӧ���ü����Ȼ�狀��������ƹ���ķ�������ֻ�����Ȼ�粒��岻�ܵõ�������A����
B.![]() Ϊ������ԭ��Ӧ��
Ϊ������ԭ��Ӧ��![]() Ϊ������������Ϊ��ԭ�������������ͻ�ԭ�������ʵ���֮��Ϊ3:2��B����
Ϊ������������Ϊ��ԭ�������������ͻ�ԭ�������ʵ���֮��Ϊ3:2��B����
C.װ��B������Ϊ���ﰱ������������ʿ����Ǽ�ʯ�ң���������ˮ�Ȼ��ƣ����백���������������C����
D. D����ȴ����Һ��Ϊˮ�Ͱ���������Һ�Լ��ԣ���D��Һ�����ʹ����ĺ�ɫʯ����ֽ������D��ȷ��
��ѡD��

 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�����Ŀ���������Ĺ̶��Ǽ���������ѧ��һֱ�о��Ŀ��⡣
��1���±��о��˲�ͬ�¶��´����̵���ҵ�̵��IJ���Kֵ��
��Ӧ | �����̵� N2��g����O2��g�� | ��ҵ�̵� N2��g����3H2��g�� | |||
�¶�/�� | 27 | 2000 | 25 | 400 | 450 |
K | 3.8��10��31 | 0.1 | 5��108 | 0.507 | 0.152 |
���������ݿ�֪�������̵���Ӧ����_____��������������������������Ӧ��
���������ݿ�֪������ʺϴ��ģģ������̵���ԭ��__________________________��
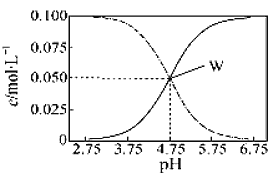
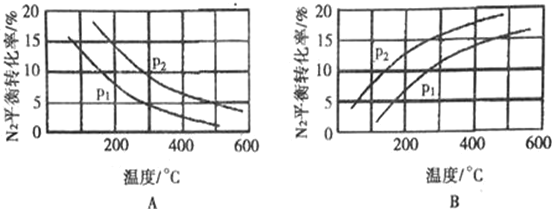
��2����ҵ�̵���Ӧ�У�������������ͬʱ���ֱ�ⶨN2��ƽ��ת�����ڲ�ͬѹǿ��P1��P2�������¶ȱ仯�����ߣ���ͼ��ʾ��ͼʾ�У���ȷ����___������A������B�������Ƚ�P1��P2�Ĵ�С��ϵ��P1______P2(������������� ����)��
���� Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��![]() 2NH3��g��
2NH3��g��
��3����һ���¶��£���1mol N2��3mol H2����������������ܱ������з�����Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8mol����ƽ��ʱ��H2��ת������1��____��
����Ŀ��I�����ݱ�����Ϣ����ش��������⣺
��ѧ��Ӧ | ƽ�ⳣ�� | �¶� | |
973K | 1173K | ||
��Fe(s)��CO2(g) | K1 | 1.47 | 2.15 |
��Fe(s)��H2O(g) | K2 | 2.38 | 1.67 |
��CO(g)��H2O(g) | K3 | �� | �� |
(1)��Ӧ����________(��������������������)��Ӧ��
(2)д����Ӧ�۵�ƽ�ⳣ��K3�ı���ʽ_______________________��
(3)���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3��________(��K1��K2��ʾ)��
(4)Ҫʹ��Ӧ����һ�������½�����ƽ�����淴Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��____(��д��ĸ���)��
A����С��Ӧ�������ݻ�B������Ӧ�������ݻ�
C�������¶�D��ʹ�ú��ʵĴ���
E���跨��Сƽ����ϵ�е�COŨ��
(5)����Ӧ�۵��淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��
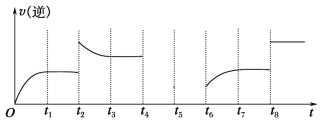
�ٿɼ���Ӧ��t1��t3��t7ʱ���ﵽ��ƽ�⣬��t2��t8ʱ���ı���һ�����������жϸı����ʲô������t2ʱ________��t8ʱ________��
����t4ʱ��ѹ��t6ʱ����Ӧ���Ũ�ȣ�����ͼ�л���t4��t6ʱ�淴Ӧ������ʱ��Ĺ�ϵ���ߡ�__________
����25����1.01��105Paʱ��16gҺ̬�״�(CH3OH)��ȫȼ�գ����ָ���ԭ״̬ʱ���ų�363.3kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ__________
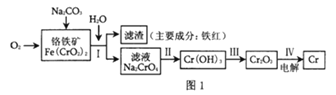
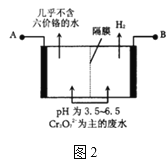
����Ŀ����ҵ�ϻ�������ij�Ͻ���ϣ���Ҫ��Fe��Cu��Co��Li�ȣ���֪Co��Fe�����еȻ��ý������Ĺ����������£�
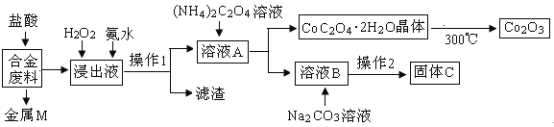
��1������MΪ__________������1Ϊ___________��
��2������H2O2�������ǣ������ӷ���ʽ��ʾ��________�����백ˮ��������________��
��3����ֱ��յĻ�ѧ����ʽΪ____________��
��4����֪Li2CO3����ˮ���䱥����Һ��Ũ�����¶ȹ�ϵ���±�������2�У�����Ũ���������ȹ��ˣ���ԭ����___________��90��ʱKsp��Li2CO3����ֵΪ___________��
�¶�/�� | 10 | 30 | 60 | 90 |
Ũ��/molL��1 | 0.21 | 0.17 | 0.14 | 0.10 |
��5���ö��Ե缫�������Li2CO3��ȡﮣ����������������壬�������ĵ缫��ӦʽΪ__________��