题目内容
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 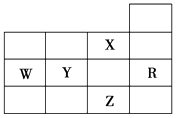
A.W元素的电负性大于Y元素的电负性
B.X元素是电负性最大的元素
C.p能级未成对电子最多的是Z元素
D.Y,Z的阴离子电子层结构都与R原子的相同
【答案】B
【解析】解:由元素在周期表的位置可知,X为F,W为P,Y为S,R为Ar,Z为Br, A.非金属性S>P,W元素的电负性小于Y元素的电负性,故A错误;
B.F的非金属性最强,则X元素是电负性最大的元素,故B正确;
C.p能级未成对电子最多为3个,则p能级未成对电子最多的是W元素,故C错误;
D.Z的阴离子电子层结构比R原子的多1个电子层,而Y的阴离子电子层结构都与R原子的相同,故D错误;
故选B.
由元素在周期表的位置可知,X为F,W为P,Y为S,R为Ar,Z为Br,
A.非金属性越强,电负性越大;
B.F的非金属性最强;
C.p能级未成对电子最多为3个;
D.Z的阴离子电子层结构比R原子的多1个电子层.

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
(1)【观察与思考】 乙醇分子的核磁共振氢谱有个吸收峰.
(2)【活动与探究】 (i)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满).
实验现象 | 结 论 | |
① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
② |
(ii)乙同学向试管中加入3~4mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次.则此时乙醇发生反应的化学方程式为(生成乙醛) . 欲验证此实验的有机产物,可以将产物加入盛有的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为 .
(3)【交流与讨论】 丙同学向一支试管中加入3mL 乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,按下图所示连接好装置,请指出该装置的主要错误是 . 假如乙醇分子中的氧原子为18O原子,则发生此反应后,18O原子将出现在生成物中(填字母).
A.水 B.乙酸乙酯 C.水和乙酸乙酯.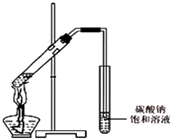
【题目】用酸式滴定管准确移取10.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20molL ﹣1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.50mL | 18.60mL |
第二次 | 0.70mL | 19.00mL |
(1)根据以上数据可以计算出盐酸的物质的量浓度为molL﹣1 .
(2)达到滴定终点的标志是 .
(3)以下操作造成测定结果偏高的原因可能是 . A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.