题目内容
【题目】乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
(1)【观察与思考】 乙醇分子的核磁共振氢谱有个吸收峰.
(2)【活动与探究】 (i)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满).
实验现象 | 结 论 | |
① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
② |
(ii)乙同学向试管中加入3~4mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次.则此时乙醇发生反应的化学方程式为(生成乙醛) . 欲验证此实验的有机产物,可以将产物加入盛有的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为 .
(3)【交流与讨论】 丙同学向一支试管中加入3mL 乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,按下图所示连接好装置,请指出该装置的主要错误是 . 假如乙醇分子中的氧原子为18O原子,则发生此反应后,18O原子将出现在生成物中(填字母).
A.水 B.乙酸乙酯 C.水和乙酸乙酯.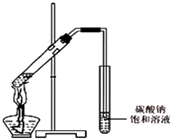
【答案】
(1)3
(2)产生气泡;钠与乙醇反应有氢气产生;![]() ;新制的氢氧化铜;CH3CHO+2Cu(OH)2
;新制的氢氧化铜;CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O
CH3COOH+Cu2O↓+2H2O
(3)导管插入到饱和碳酸钠溶液中;B
【解析】解:(1)乙醇结构简式为CH3CH2OH,分子中含有3种氢原子,所以有三个吸收峰,峰面积之比是1:2:3,所以答案是:3;(2)乙醇中含有羟基,能与金属钠反应生成氢气,乙醇的密度比钠小,金属钠沉在乙醇底部,比在水中反应安静,并不剧烈,钠粒逐渐变小,缓缓产生气泡;所以答案是:产生气泡; 钠与乙醇反应有氢气产生;(3)乙醇催化氧化生成乙醛,反应方程式为: ![]() ;
;
乙醛和新制氢氧化铜反应生成砖红色沉淀,反应方程式为:CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O,
CH3COOH+Cu2O↓+2H2O,
所以答案是: ![]() ;新制的氢氧化铜; CH3CHO+2Cu(OH)2
;新制的氢氧化铜; CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O(4)由于生成的乙酸乙酯中混有乙醇和乙酸,易溶于水,会产生倒吸现象,故伸入饱和碳酸钠的导管不能在液面下,酯化反应原理是酸脱羟基醇脱氢,故18O出现在乙酸乙酯中;
CH3COOH+Cu2O↓+2H2O(4)由于生成的乙酸乙酯中混有乙醇和乙酸,易溶于水,会产生倒吸现象,故伸入饱和碳酸钠的导管不能在液面下,酯化反应原理是酸脱羟基醇脱氢,故18O出现在乙酸乙酯中;
所以答案是:导管插入到饱和碳酸钠溶液中;B.