题目内容
14.下列说法正确的是( )| A. | H、D、T表示三种氢原子 | |
| B. | 卤族元素最高化合价均为正7价,最低化合价均为负1价 | |
| C. | 金属元素的原子最外层电子数,都少于4个 | |
| D. | 目前人们已发现了5000多种核素,说明发现了5000多种元素 |
分析 A.H、D、T是氢元素3种核素;
B.F无正化合价;
C.主族元素的金属最外层电子数少于4个;
D.同一元素存在多种核素.
解答 解:A.H、D、T质子数相同、中子数不同,是氢元素3种核素,故A正确;
B.F无正化合价,故B错误;
C.主族元素的金属最外层电子数少于4个,过渡元素(如VB、VIB等)最外层电子数均多于4个,故C错误;
D.目前只发现100多种元素,同一元素存在多种核素,核素种数远远大于元素种数,故D错误,
故选A.
点评 本题考查特殊元素原子结构特点、核素等,比较基础,侧重对基础知识的巩固.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,已知X的原子序数比Y的原子序数大,下列说法中正确的是( )
| A. | X的金属性比Y的金属性强 | |
| B. | 常温下,X和Y都不能从水中置换出氢 | |
| C. | Y元素的氢氧化物碱性比X 元素的氢氧化物碱性强 | |
| D. | X元素的最高化合价比Y 元素的最高化合价低 |
19.下列各组物质中,化学键类型完全相同的一组是( )
| A. | Na2O2和H2O2 | B. | KOH和H2SO4 | C. | CCl4和KCl | D. | MgCl2和Na2O |
11.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时B的浓度是原来的35%,则( )
| A. | 物质A的转化率大了 | B. | a<b | ||
| C. | 物质B的质量分数减小了 | D. | 平衡向正反应方向移动了 |
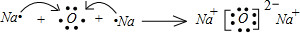
 或
或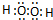
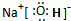
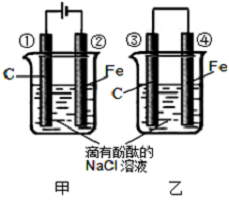 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.