题目内容
16.下列物质含少量杂质(括号内为杂质),所选用的试剂和分离方法不能达到实验目的是( )| 混合物 | 试剂 | 分离方法 | |
| A | 溴苯(溴) | 氢氧化钠 | 分液 |
| B | 乙烷(乙烯) | 氢气 | 催化剂、加热 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠 | 分液 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溴能与氢氧化钠溶液反应;
B.通氢气会混有新杂质;
C.乙酸乙酯在饱和碳酸钠中的溶解度比较小;
D.新制生石灰与水反应,可减少乙醇中水的量.
解答 解:A.溴能与氢氧化钠溶液反应,溴苯不能,然后分液即可,故A正确;
B.通氢气会混有新杂质,则除去乙烷中的乙烯时,应选择溴水及洗气法,故B错误;
C.乙酸能与碳酸钠溶液反应,且乙酸乙酯在饱和碳酸钠中的溶解度比较小,分液可以分离,故C正确;
D.新制生石灰与水反应,可减少乙醇中水的量,然后蒸馏可制备无水乙醇,故D正确.
故选B.
点评 本题考查物质的分离提纯和除杂,题目难度不大,注意把握相关物质的性质的异同,为解答该类题目的关键.

练习册系列答案
相关题目
13.已知H2(g)+Br2(g)=2HBr(g);△H=A KJ/mol,其它的相关数据如下表:
则表中a为( )
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | B | a | C |
| A. | A-B+C | B. | 2C-A-B | C. | C-A-B | D. | A-B+2C |
7.甲烷分子是以碳原子为中心的正四面体结构而不是正方形的平面结构,其理由是( )
| A. | CHCl3只有一种结构 | |
| B. | CH2Cl2只有一种结构 | |
| C. | CH4是非极性分子 | |
| D. | CH4的四个价键的键长和键能都相等 |
11.下列各项中的两种物质无论以何种比例混合,只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )
| A. | C3H6、C3H8O | B. | C3H6、C2H6O | C. | C2H2、C6H6 | D. | CH4O、C2H4O3 |
1.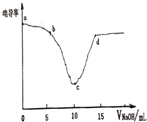 电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )
电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )
 电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )
电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )| A. | d点溶液中:c(Cl-)=2c(OH-)-2c(H+) | |
| B. | 电导率传感器能用于酸碱中和滴定终点的判断 | |
| C. | c点电导率最小是因为c点溶液的溶质为弱电解质 | |
| D. | c(Na+)、c(Cl-)对导电能力的影响比c(H+)、c(OH-)对导电能力的影响小 |
8.下列物质中,既有离子键,又有共价键的是( )
| A. | CaCl2 | B. | NaOH | C. | H2O | D. | Na2O |
5.类推是学习和研究化学的重要思维方法.下列类推结论正确的是( )
| A. | 向Ba(NO3)2溶液中通入CO2不产生白色沉淀,则通入SO2也不产生白色沉淀 | |
| B. | 电负性:C<N<O,则第一电离能:C<N<O | |
| C. | 乙醛能被新制Cu(OH)2氧化,则乙醛也能被溴水氧化 | |
| D. | HBr的沸点小于HI的沸点,则HBr的稳定性小于HI的稳定性 |
6.有关物质性质及用途的说法,正确的是( )
| A. | 甲烷与氯气在光照的条件下制取纯净的一氯甲烷 | |
| B. | 常见的塑料有:①聚乙烯 ②聚丙烯 ③聚氯乙烯 ④聚苯乙烯,其分子内部都含有双键 | |
| C. | 牡丹籽油是一种优良的植物油脂,它可使酸性高锰酸钾溶液褪色 | |
| D. | 等质量的乙烯和聚乙烯充分燃烧所需氧气的量不相等 |
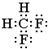 ;下列对于乙的描述正确的是d.
;下列对于乙的描述正确的是d.