题目内容
11.下列各项中的两种物质无论以何种比例混合,只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )| A. | C3H6、C3H8O | B. | C3H6、C2H6O | C. | C2H2、C6H6 | D. | CH4O、C2H4O3 |
分析 只要混合物的总物质的量一定,完全燃烧消耗O2的质量保持不变,则1mol各组分消耗氧气的量相等;总物质的量一定生成水的质量不变,则有机物分子中含有的H原子数目一定相等,据此进行解答.
解答 解:混合物的总物质的量一定,完全燃烧生成水的质量和消耗O2的质量均不变,则1mol各组分消耗氧气的量相等,分子中含有的氢原子数目相等,
A.C3H6、C3H8O分子中含有的氢原子分别为6、8,二者含有的氢原子数不同,则不同比例混合后生成水的量不同,故A错误;
B.1molC3H6完全反应消耗4.5mol氧气,而1molC2H6O完全反应消耗3mol氧气,所以1molC3H6与1molC2H6O耗氧量不相同,不符合题意,故B错误;
C.C2H2、C6H6最简式相同,1molC6H6的耗氧量为1molC2H2耗氧量的3倍,且分子中含有的H数目不同,物质的量一定时二者比例不同,生成水的量不同,故C错误;
D.C2H4O3改写为CH4O•CO2,CH4O、C2H4O3分子中含有H原子数相等,且1mol时消耗的氧气都是1.5mol,所以只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变,故D正确;
故选D.
点评 本题考查混合物计算、有机物分子式确定,题目难度中等,注意根据燃烧通式理解烃及其含氧衍生物耗氧量问题,注意D利用改写法进行比较,可简化计算过程.

练习册系列答案
相关题目
2. 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )| A. | O2在电极b上发生还原反应 | |
| B. | 溶液中OH-向电极a移动 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | 负极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O |
19.一定温度下,难溶电解质的饱和溶液中存在着沉淀溶解平衡,已知:
25℃时,对于含Fe2(SO4)3、FeSO4和CuSO4各0.5mol的1L,混合溶液,根据如表数据断,下列说法不正确的是( )
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| KSP(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| A. | 在pH=5的溶液中.Fe3+不能大量存在 | |
| B. | 混合溶液中c(SO42-):[c(Fe3+)+c(Fe2+)+c(Cu2+)]>5:4 | |
| C. | 向混合溶液中逐滴加入0.1mol•L-1NaOH溶液,最先看到红褐色沉淀 | |
| D. | 向混合溶液中加入适量氯水,并调节pH到3~4过滤,可获较纯净的CuSO4溶液 |
6.化学与生活密切相关,下列说法正确的是( )
| A. | 福尔马林可用作食品防腐剂 | |
| B. | 苯酚皂可用于环境消毒,医用酒精可用于皮肤消毒,其原因是它们都可以杀死细菌 | |
| C. | “乙醇汽油”是在汽油中加入乙醇生成的一种新化合物 | |
| D. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 |
16.下列物质含少量杂质(括号内为杂质),所选用的试剂和分离方法不能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 溴苯(溴) | 氢氧化钠 | 分液 |
| B | 乙烷(乙烯) | 氢气 | 催化剂、加热 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠 | 分液 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
3.元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于S2-的半径,X元素为( )
| A. | Al | B. | P | C. | K | D. | Ar |
20.只用水就能鉴别的一组物质是( )
| A. | 苯、乙酸、四氯化碳 | B. | 乙醇、乙醛、乙酸 | ||
| C. | 溴苯、乙二醇、硝基苯 | D. | 乙酸乙酯、乙醇、甘油 |
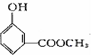
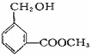
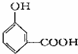
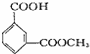
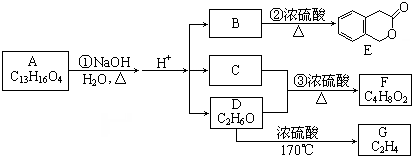
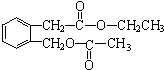 ;B的分子式是C9H10O3.
;B的分子式是C9H10O3. 、
、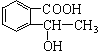 、
、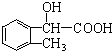 .
. .
.