题目内容
【题目】下列酸碱溶液恰好完全中和,如图所示,则下列叙述正确的是
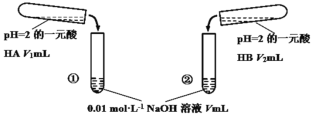
A.因为两种酸溶液的pH相等,故V1一定等于V2
B.若V1>V2,则说明HA为强酸,HB为弱酸
C.若实验①中,V=V1,则混合液中c(Na+)=c(A-)
D.实验②的混合溶液,可能溶液呈酸性
【答案】C
【解析】
因为题干中给出信息“下列酸碱溶液恰好完全中和”,所以c(HA)![]() V1=c(HB)
V1=c(HB)![]() V2。
V2。
A.因为不知道两种酸的酸性强弱关系,所以不能判断V1与V2的相对大小,A错误;
B.V1>V2,代入c(HA)![]() V1=c(HB)
V1=c(HB)![]() V2,可知c(HA)<c(HB),因为HA与HB的pH相等,所以HA的酸性比HB强,但不一定是强酸,B错误;
V2,可知c(HA)<c(HB),因为HA与HB的pH相等,所以HA的酸性比HB强,但不一定是强酸,B错误;
C.若实验①中,V=V1,说明HA的物质的量浓度也为0.01mol/L,其pH=2,则HA为强酸,所以反应后是强酸强碱盐,溶液显中性,根据电荷守恒混合液中c(Na+)=c(A-),C正确;
D.完全反应后实验②的混合溶液中溶质为强碱弱酸盐或强酸强碱盐,溶液为碱性或者中性,不可能呈酸性,D错误;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目