题目内容
银锌电池广泛用作各种电子仪器的电源,其电极分别是Ag2O和锌,电解液为KOH溶液。电池反应是:Ag2O+Zn+H2O="2Ag" +Zn(OH)2,根据上述判断:
(1)原电池的正极是__________,负极是__________。
(2)原电池电极反应式为:负极_______________,正极______________。
(3)工作时原电池负极附近溶液的pH__________ (填“增大”、“不变”、“减小”)。
(1)原电池的正极是__________,负极是__________。
(2)原电池电极反应式为:负极_______________,正极______________。
(3)工作时原电池负极附近溶液的pH__________ (填“增大”、“不变”、“减小”)。
(5分)(1)Ag2O, Zn。
(2)Zn+ 2OH--2e-=Zn(OH)2;Ag2O+H2O+2e-=2Ag+ 2OH-。 (3)减小
(2)Zn+ 2OH--2e-=Zn(OH)2;Ag2O+H2O+2e-=2Ag+ 2OH-。 (3)减小
试题分析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据方程式可知,锌失去电子,作负极。氧化银得到电子,做正极。
(2)负极锌失去电子,电极反应式是Zn+ 2OH--2e-=Zn(OH)2。正极氧化银得到电子,电极反应式是Ag2O+H2O+2e-=2Ag+ 2OH-。
(3)根据负极电极反应式可知,工作时原电池负极消耗OH-,所以附近溶液的pH减小。
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固,难度不大。该题的关键是明确原电池的工作原理,有利于培养学生的逻辑推理能力和发散思维能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 Li2FeSiO4 +Li2SO4 +SiO2
Li2FeSiO4 +Li2SO4 +SiO2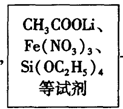
 Li2FeSiO4
Li2FeSiO4 Li2FeSiO4则该电池的负极是____ ;充电时,阳极反应的电极反应式为 ;
Li2FeSiO4则该电池的负极是____ ;充电时,阳极反应的电极反应式为 ;