��Ŀ����
14�� �ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��Ϊ��
�ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��Ϊ��N2��g��+3H2��g���T2NH3��g����H=-92.4kJ•mol-1һ�ֹ�ҵ�ϳɰ��ļ�������ͼ���£�
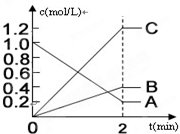
��1�����ܱ������У�ʹ2mol N2��6mol H2��Ϸ������з�Ӧ��N2��g��+3H2��g���T2NH3��g��������ӦΪ���ȷ�Ӧ��
����Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ���1��3������ƽ����ϵ���¶ȣ�����������䣩��
��������ƽ����Է���������С����������С�����䡱��
��2����Ȼ���е�H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������д��������Ӧ�Ļ�ѧ����ʽ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S����
��3���������������ԭ�����£�
��CH4��g��+H2O��g���TCO��g��+3H2��g����H=+206.4kJ•mol-1
��CO��g��+H2O��g���TCO2��g��+H2��g����H=-41.2kJ•mol-1
���ڷ�Ӧ�٣�һ���������ƽ����ϵ��H2�ٷֺ��������ܼӿ췴Ӧ���ʵĴ�ʩ��a��
a�������¶ȡ�b������ˮ����Ũ��c��������� d������ѹǿ
���÷�Ӧ�ڣ���CO��һ��ת���������H2��������a mol CO��H2�Ļ�����壨H2���������Ϊ80%����H2O��Ӧ���õ�1.14a mol CO��CO2��H2�Ļ�����壬��COת����Ϊ70%��
��4����������ͼ�У�ʹ�ϳɰ��ų��������õ�������õ���Ҫ�����ǣ�����ţ�����ԭ������ѹ����������������ߺϳɰ�ԭ����ת���ʵķ���������Һ����δ��Ӧ��N2��H2ѭ��ʹ�ã�
���� ��1��������ʼ���������������ʵ���֮�ȵ��ڷ�Ӧ֮�ȷ����жϣ���Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У������������䣬���ʵ���������M=$\frac{m}{n}$�жϣ�
��2��H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ��������Ӧ����������һˮ�ϰ�������ԭ���غ�͵����غ���ƽ��д��ѧ����ʽ��
��3����Ӧ�������������������ȷ�Ӧ��һ���������ƽ����ϵ��H2�ٷֺ�����˵��ƽ��������У����ܼӿ췴Ӧ���ʣ�˵��Ӱ�췴Ӧ���ʵ��������������¡���ѹ������Ũ�ȵȣ�������Ӧ������֪��Ӧ��������ҷ�Ӧ���������ֻ������ƽ�������ȷ�Ӧ���У�ƽ��������з�Ӧ������������ƽ���ƶ�ԭ����Ӱ�췴Ӧ�������ط����жϣ����ݻ�ѧƽ������ʽ��ʽ���㣬����ת���ʵı���ʽ���㣻
��4�����ݷ�Ӧ�����������С�ķ��ȷ�Ӧ�����ƽ���ƶ�ԭ�������жϣ�
��� �⣺��1��������ʼ���������������ʵ���֮�ȵ��ڷ�Ӧ֮�ȷ����жϣ����ܱ������У�ʹ2molN2��6molH2��Ϸ������з�Ӧ��N2��g��+3H2��g��?2NH3��g������Ӧ����ʼ��֮�ȵ��ڻ�ѧ����ʽ�еķ�Ӧ֮�ȣ�����ƽ��Ũ��Ϊ1��3��N2��g��+3H2��g��?2NH3��g��������ӦΪ���ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����������ƽ��������У������������䣬�������ʵ�������M=$\frac{m}{n}$��֪����������ƽ����Է���������С���ʴ�Ϊ��1��3����С��
��2��H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ��������Ӧ����������һˮ�ϰ�������ԭ���غ�͵����غ���ƽ��д��ѧ����ʽΪ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S�����ʴ�Ϊ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S����
��3����Ӧ��CH4��g��+H2O��g��?CO2��g��+3H2��g����H=+206.4 kJ•mol-1�������������������ȷ�Ӧ��һ���������ƽ����ϵ��H2�ٷֺ�����˵��ƽ��������У����ܼӿ췴Ӧ���ʣ�˵��Ӱ�췴Ӧ���ʵ��������������¡���ѹ������Ũ�ȵȣ�������Ӧ������֪��Ӧ��������ҷ�Ӧ���������ֻ������ƽ�������ȷ�Ӧ���У�ƽ��������з�Ӧ��������
a����Ӧ�����ȷ�Ӧ�������¶ȣ���Ӧ��������ƽ��������У�ƽ����ϵ��H2�ٷֺ�������a��ȷ��
b������ˮ����Ũ�ȣ�ƽ��������У���Ӧ��������ƽ����ϵ��H2�ٷֺ�����һ������b����
c������������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬��Ӧ�������������ٷֺ������䣬��c����
d����Сѹǿ��ƽ�����������ƶ��������ٷֺ���������Ӧ���ʼ�С����d����
���÷�Ӧ�ڣ���CO��һ��ת���������H2����������amol CO��H2�Ļ�����壨H2���������Ϊ80%���� H2Ϊ��amol��80%=0.8amol��CO�����ʵ���Ϊ��0.2amol����H2O��Ӧ���õ�1.14amol CO��CO2��H2�Ļ�����壬�÷�Ӧǰ������������䣬���ӵIJ���Ӧ������ʼ��ˮ���������ʵ���Ϊ��1.14amol-amol=0.14amol��
��ת����һ����̼�����ʵ���Ϊx����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 0.2a 0.14a 0 0.8a
�仯����mol�� x x x x
ƽ������mol��0.2a-x 0.14a-x x x+0.8a
��0.2a-x+x+x+0.8a=1.14a��
x=0.14amol
��COת����Ϊ��$\frac{0.14amol}{0.2a\\;mol}$��100%=70%��
�ʴ�Ϊ��a��70%��
��4�������̺ϳɰ�����ͨ�����Ƚ��������ȷ�Ӧ������壬ʹ��Ӧ�ﵽ�����¶ȣ���ߺϳɰ�ԭ����ת���ʣ�����ƽ���ƶ�ԭ������������������ٽ�ƽ��������У���ƽ���������е�������������ѭ��ʹ�ã����ԭ�������ʣ�
�ʴ�Ϊ������ԭ������ѹ������Һ����δ��Ӧ��N2��H2ѭ��ʹ�ã�
���� ���⿼���˻�ѧƽ��Ӱ�����ء���ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ�ע�⻯ѧƽ��ļ��㷽������ȷ��ѧƽ�⼰��Ӱ�����أ�����������ѧ���ķ�����������������ѧ����������

| A�� | FeO+HNO3����Һ�� | B�� | ������+ϡ���� | ||
| C�� | FeCl3����Һ��+������ | D�� | Fe+CuSO4����Һ�� |
| A�� | 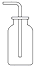 Cl2���ռ� | B�� | 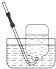 HCl���ռ� | C�� |  NH3���ռ� | D�� | 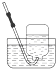 NO���ռ� |
| A�� | ��H��0��ʾ���ȷ�Ӧ����H��0��ʾ���ȷ�Ӧ | |
| B�� | ��Ӧ��������ʴ��ڷ�Ӧ�������ʱ����H��0 | |
| C�� | ��H�Ĵ�С���Ȼ�ѧ����ʽ�еĸ����ʵĻ�ѧ�������� | |
| D�� | �ڻ�ѧ��Ӧ�У��������ʱ仯��ͬʱ��һ�����������仯 |
| A�� | Ԫ�����ڱ��У�����һ�͵��������⣬��n���������ǽ���Ԫ�ص�������Ϊ��8-n�� | |
| B�� | SiCl4��PCl3�����и�ԭ���������ﵽ8�����ȶ��ṹ | |
| C�� | ��̬�⻯���ˮ��Һ������ | |
| D�� | ��A��͢�A��Ԫ���γɵ�ԭ�Ӹ�����1��1����������38�Ļ�������й��ۼ������ӻ����� |
| A�� | ������N2��NO2�Ļ������ | B�� | ������N2��NO�Ļ������ | ||
| C�� | ������NO��NO2�Ļ������ | D�� | ������NO2һ������ |

 ��1��Ǧ�����dz��õĻ�ѧ��Դ����缫������Pb��PbO2�����ҺΪϡ���ᣮ����ʱ�õ���ܷ�ӦʽΪPbO2+Pb+2H2SO4�T2PbSO4+2H2O���ݴ��жϣ�
��1��Ǧ�����dz��õĻ�ѧ��Դ����缫������Pb��PbO2�����ҺΪϡ���ᣮ����ʱ�õ���ܷ�ӦʽΪPbO2+Pb+2H2SO4�T2PbSO4+2H2O���ݴ��жϣ�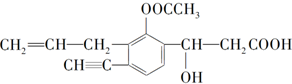 ij�л�������ṹ��ʽΪ
ij�л�������ṹ��ʽΪ