题目内容
9.下列说法中正确的是( )| A. | △H>0表示放热反应,△H<0表示吸热反应 | |
| B. | 反应产物的总焓大于反应物的总焓时,△H>0 | |
| C. | △H的大小与热化学方程式中的各物质的化学计量数无关 | |
| D. | 在化学反应中,发生物质变化的同时不一定发生能量变化 |
分析 A、放热反应的焓变小于0;
B、反应物总能量高于生成物时,反应放热;
C、△H的数值与化学计量数对应,随化学计量数的改变而改变;
D、化学反应过程就是旧化学键断裂新化学键形成过程,断裂化学键需吸收能量,形成化学键会释放能量.
解答 解:A、△H=Q(生成物的能量和)-Q(反应物的能量和),反应物能量高时△H<0反应放热,反之△H>0反应吸热,故A错误;
B、△H=Q(生成物的能量和)-Q(反应物的能量和),所以△H>0时,反应产物的总焓大于反应物的总焓,故B正确;
C、△H的数值与化学计量数对应,随化学计量数的改变而改变,故C错误;
D、化学反应过程就是旧化学键断裂新化学键形成过程,断裂化学键需吸收能量,形成化学键会释放能量,所以,任何化学反应一定有能量变化,故D错误;
故选B.
点评 本题考查化学反应中能量变化与化学键的关系,以及△H的求算,题目难度不大,注意△H=Q(生成物的能量和)-Q(反应物的能量和).

练习册系列答案
相关题目
20.一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相同,将 1.0L这种混合气体在氧气中充分燃烧,生成2.0LCO2和2.4L水蒸气(相同条件下测定).则混合物中烷烃和烯烃的体积比为( )
| A. | 3:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
17. (1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:
(1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:
$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
该反应的平衡常数表达式K=$\frac{[C{O}_{2}]}{[CO]}$,△H<0(填“>”、“<”或“=”);
(2)工业上CO 也用于合成甲醇:
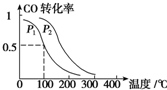
CO(g)+2H2(g)?CH3OH(g)△H=-90.1kJ•mol-1.一定压强下,向容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.
①p1小于p2(填“大于”、“小于”或“等于”);
②100℃时,该反应的化学平衡常数K=$(\frac{V}{a})^{2}$(mol•L-1)-2;
③保持其它条件不变,下列措施中能够增大上述合成甲醇反应的反应速率、且能提高CO转化率的是cd.(填字母).
a.使用高效催化剂 b.降低反应温度 c.通入H2d.再增加a mol CO和2a molH2 e.不断将CH3OH从反应混合物中分离出来.
 (1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:
(1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)工业上CO 也用于合成甲醇:
CO(g)+2H2(g)?CH3OH(g)△H=-90.1kJ•mol-1.一定压强下,向容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.
①p1小于p2(填“大于”、“小于”或“等于”);
②100℃时,该反应的化学平衡常数K=$(\frac{V}{a})^{2}$(mol•L-1)-2;
③保持其它条件不变,下列措施中能够增大上述合成甲醇反应的反应速率、且能提高CO转化率的是cd.(填字母).
a.使用高效催化剂 b.降低反应温度 c.通入H2d.再增加a mol CO和2a molH2 e.不断将CH3OH从反应混合物中分离出来.
1.下列各项不属于官能团的是( )
| A. | NO${\;}_{3}^{-}$ | B. | -Cl | C. | 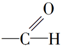 | D. | -NO2 |
19.在一定条件下RO3-与R-发生如下反应:RO3-+5R-+6H+=3R2+3H2O,则下列关于R元素的说法中正确的是( )
| A. | R位于元素周期表中的第VA族 | B. | R位于元素周期表中的第 VIIA族 | ||
| C. | RO3-中的R元素只能被还原 | D. | R2在常温常压下一定是气体 |
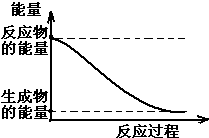 (1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热.(填“吸热”或“放热”)反应,NO2和CO的总能量大于(填
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热.(填“吸热”或“放热”)反应,NO2和CO的总能量大于(填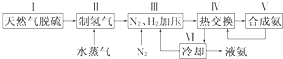 合成氨是人类科学技术上的一项重大突破,其反应原理为:
合成氨是人类科学技术上的一项重大突破,其反应原理为: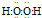 .
.