题目内容
13.丹参素能明显抑制血小板的聚集,其结构如图所示,下列说法错误的是( )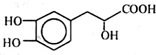
| A. | 丹参素的分子式为C9H10O5 | |
| B. | 1 mol丹参素最多可以和4 mol H2发生加成反应 | |
| C. | 1 mol丹参素在一定条件下与足量金属钠反应可生成2 mol H2 | |
| D. | 丹参素能发生取代、中和、氧化反应等反应 |
分析 该分子中含有酚羟基、苯环、醇羟基和羧基,具有酚、苯、醇和羧酸的性质,能发生取代反应、氧化反应、还原反应、加成反应、消去反应、酯化反应、中和反应等,据此分析解答.
解答 解:A.根据结构简式知,丹参素的分子式为C9H10O5,故A正确;
B.苯环能和氢气发生加成反应,所以1 mol丹参素最多可以和3mol H2发生加成反应,故B错误;
C.酚羟基、醇羟基和羧基能和钠反应生成氢气,所以1 mol丹参素在一定条件下与足量金属钠反应可生成2 mol H2,故C正确;
D.该分子中含有酚羟基、苯环、醇羟基和羧基,具有酚、苯、醇和羧酸的性质,能发生取代反应、氧化反应、还原反应、加成反应、消去反应、酯化反应、中和反应等,故D正确;
故选B.
点评 本题考查有机物结构和性质,为高频考查,明确官能团及其性质关系是解本题关键,侧重考查酚、苯、醇和羧酸的性质,.

练习册系列答案
相关题目
4.生活中处处有化学,下列说法不正确的是( )
| A. | 采用原煤脱硫技术,可减少燃煤时产生的SO2 | |
| B. | 食品中适量添加防腐剂,可以保障安全 | |
| C. | 垃圾分为可回收物、厨余垃圾、有害垃圾、其它垃圾等,废旧电池属于可回收垃圾 | |
| D. | 用红薯酿酒的过程中包含氧化还原反应 |
8.SO2通入足量的Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀.针对上述一系列变化,下列说法错误的是( )
| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述反应可知氧化性HNO3>Fe3+>稀硫酸 | |
| C. | 上述过程中,会产生一种无色、难溶于水的气体 | |
| D. | 若通入的SO2完全反应,则通入的SO2和逸出的气体物质的量之比为1:1 |
18.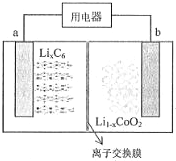 某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )
某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )
 某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )
某聚合物锂离子充电电池放电时的反应为:Li1-xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是( )| A. | 放电时,电子从b极流向a极 | |
| B. | 放电时,a极脱出的离子通过阴离子交换膜从左向右移动 | |
| C. | 充电时,b极发生的反应为:LiCoO2-xe-=Li1-xCoO2+xLi+ | |
| D. | 充电时,每转移x mol 电子,产生6mol碳单质 |
20.生活中的一些问题常涉及到化学知识,下列叙述不正确的是( )
| A. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| B. | “加碘食盐”、“含氟牙膏”、“富硒营养品”、“高钙牛奶”、“加铁酱油”等等,这里的碘、氟、硒指的是化合物,钙、铁则分别是Ca2+和Fe3+ | |
| C. | 发生地震后,防疫人员在震区周围撒石灰,进行环境消毒,防止灾后出现疫情 | |
| D. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁等还原性物质 |
20.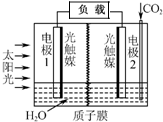 利用人工模拟光合作用合成甲酸的原理为:
利用人工模拟光合作用合成甲酸的原理为:
太阳能光触媒2CO2+2H2O $→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
 利用人工模拟光合作用合成甲酸的原理为:
利用人工模拟光合作用合成甲酸的原理为:太阳能光触媒2CO2+2H2O $→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
| A. | 电极1周围pH增大 | |
| B. | 电子由电极1经过负载流向电极2 | |
| C. | 电极2的反应式:CO2+2H++2e-=HCOOH | |
| D. | 该装置能将太阳能转化为化学能和电能 |
 含硅元素的化合物广泛存在于自然界中,与其他矿物共同构成岩石.晶体硅(熔点 1410℃)用途广泛,制取与提纯方法有多种.
含硅元素的化合物广泛存在于自然界中,与其他矿物共同构成岩石.晶体硅(熔点 1410℃)用途广泛,制取与提纯方法有多种.