题目内容
【题目】Zn是一种应用广泛的金属。用闪锌矿(主要成分为ZnS,还含有SiO2和少量FeS、CdS、PbS、砷化合物杂质等)为原料制备金属Zn和ZnSO4·7H2O的流程如图所示:

①相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
②FeAsO4难溶于水;ZnSO4·7H2O易溶于水,难溶于酒精。
回答下列问题:
(1)滤渣1的主要成分除SiO2外还有______,焙烧后产生的气体对环境造成的常见危害为______。
(2)氧化除杂工序中加入ZnO的作用是___________。
(3)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用的试剂为____________。
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为___________。不能省去“还原除杂”步骤,直接在“氧化除杂”步骤中除去Cd2+,理由是________。
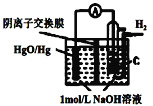
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为_____________;沉积锌后的电解液可返回______工序继续使用。
(6)酸浸液中砷元素以AsO33-存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,写出该反应的离子方程式为___________。
【答案】PbSO4 酸雨 调节溶液的pH使Fe3+沉淀完全 酒精(或饱和硫酸锌溶液) Zn+Cd2+= Zn2++Cd 在氧化除杂工序中加ZnO是为了调节溶液pH,若要完全除去Cd2+,溶液的pH至少需要调节为9.4,此时Zn2+也会完全沉淀 Ni(OH)2-e- +OH- = NiO(OH)+H2O 酸浸 5Fe2+ + 5AsO33- +3MnO4- + 14H+ = 3Mn2+ +5FeAsO4↓+7H2O
【解析】
焙烧过程中发生的反应有2ZnS+3O2![]() 2ZnO+2SO2、4FeS+7O2
2ZnO+2SO2、4FeS+7O2![]() 2Fe2O3+4SO2、2PbS+3O2
2Fe2O3+4SO2、2PbS+3O2![]() 2PbO+2SO2、2CdS+3O2
2PbO+2SO2、2CdS+3O2![]() 2CdO+2SO2,焙烧过程中生成的气体是SO2,焙烧后的主要成分变为ZnO,还存在少量的SiO2、Fe2O3、PbO、CdO,加稀硫酸后,发生一系列反应,ZnO、Fe2O3、PbO、CdO与稀硫酸反应分别生成硫酸锌、硫酸铁、硫酸铅、硫酸镉,其中SiO2和PbSO4不溶于水,以沉淀的形式沉降下来,所以滤渣1的主要成分是SiO2和PbSO4,氧化除杂工序中加入ZnO的作用是调节溶液的pH在2.8~6.2,使Fe3+完全转化为氢氧化铁沉淀,且不引入杂质,加入酸性高锰酸钾溶液能使溶液中的Fe2+转变为Fe3+,有利于除杂,同时根据第(6)酸浸液中砷元素以AsO33-存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,可知滤渣2为Fe(OH)3、FeAsO4,由第(4)问可知,还原除杂工序加入锌粉,可以还原Cd2+为金属Cd,则滤渣3为Cd以及过量的锌粉,则得到的滤液为含硫酸锌的溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥、得到ZnSO4·7H2O,经过电解得到金属Zn,据此分析解答。
2CdO+2SO2,焙烧过程中生成的气体是SO2,焙烧后的主要成分变为ZnO,还存在少量的SiO2、Fe2O3、PbO、CdO,加稀硫酸后,发生一系列反应,ZnO、Fe2O3、PbO、CdO与稀硫酸反应分别生成硫酸锌、硫酸铁、硫酸铅、硫酸镉,其中SiO2和PbSO4不溶于水,以沉淀的形式沉降下来,所以滤渣1的主要成分是SiO2和PbSO4,氧化除杂工序中加入ZnO的作用是调节溶液的pH在2.8~6.2,使Fe3+完全转化为氢氧化铁沉淀,且不引入杂质,加入酸性高锰酸钾溶液能使溶液中的Fe2+转变为Fe3+,有利于除杂,同时根据第(6)酸浸液中砷元素以AsO33-存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,可知滤渣2为Fe(OH)3、FeAsO4,由第(4)问可知,还原除杂工序加入锌粉,可以还原Cd2+为金属Cd,则滤渣3为Cd以及过量的锌粉,则得到的滤液为含硫酸锌的溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥、得到ZnSO4·7H2O,经过电解得到金属Zn,据此分析解答。
焙烧过程中发生的反应有2ZnS+3O2![]() 2ZnO+2SO2、4FeS+7O2
2ZnO+2SO2、4FeS+7O2![]() 2Fe2O3+4SO2、2PbS+3O2
2Fe2O3+4SO2、2PbS+3O2![]() 2PbO+2SO2、2CdS+3O2
2PbO+2SO2、2CdS+3O2![]() 2CdO+2SO2,焙烧过程中生成的气体是SO2,焙烧后的主要成分变为ZnO,还存在少量的SiO2、Fe2O3、PbO、CdO,加稀硫酸后,发生一系列反应,ZnO、Fe2O3、PbO、CdO与稀硫酸反应分别生成硫酸锌、硫酸铁、硫酸铅、硫酸镉,其中SiO2和PbSO4不溶于水,以沉淀的形式沉降下来,所以滤渣1的主要成分是SiO2和PbSO4,氧化除杂工序中加入ZnO的作用是调节溶液的pH在2.8~6.2,使Fe3+完全转化为氢氧化铁沉淀,且不引入杂质,加入酸性高锰酸钾溶液能使溶液中的Fe2+转变为Fe3+,有利于除杂,同时根据第(6)酸浸液中砷元素以AsO33-存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,可知滤渣2为Fe(OH)3、FeAsO4,由第(4)问可知,还原除杂工序加入锌粉,可以还原Cd2+为金属Cd,则滤渣3为Cd以及过量的锌粉,则得到的滤液为含硫酸锌的溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥、得到ZnSO4·7H2O,经过电解得到金属Zn,
2CdO+2SO2,焙烧过程中生成的气体是SO2,焙烧后的主要成分变为ZnO,还存在少量的SiO2、Fe2O3、PbO、CdO,加稀硫酸后,发生一系列反应,ZnO、Fe2O3、PbO、CdO与稀硫酸反应分别生成硫酸锌、硫酸铁、硫酸铅、硫酸镉,其中SiO2和PbSO4不溶于水,以沉淀的形式沉降下来,所以滤渣1的主要成分是SiO2和PbSO4,氧化除杂工序中加入ZnO的作用是调节溶液的pH在2.8~6.2,使Fe3+完全转化为氢氧化铁沉淀,且不引入杂质,加入酸性高锰酸钾溶液能使溶液中的Fe2+转变为Fe3+,有利于除杂,同时根据第(6)酸浸液中砷元素以AsO33-存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,可知滤渣2为Fe(OH)3、FeAsO4,由第(4)问可知,还原除杂工序加入锌粉,可以还原Cd2+为金属Cd,则滤渣3为Cd以及过量的锌粉,则得到的滤液为含硫酸锌的溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥、得到ZnSO4·7H2O,经过电解得到金属Zn,
(1)由以上分析可知,滤渣1的主要成分除SiO2外还有PbSO4;焙烧后产生的气体为SO2,其对环境造成的常见危害为酸雨,故答案为:PbSO4;酸雨;
(2)由以上分析知,氧化除杂工序中加入ZnO的作用是调节溶液的pH在2.8~6.2,使Fe3+完全转化为氢氧化铁沉淀,且不引入杂质,故答案为:调节溶液的pH使Fe3+沉淀完全;
(3)已知ZnSO4·7H2O易溶于水,难溶于酒精,则为了减少洗涤过程中晶体的损失,可以用酒精或者饱和硫酸锌溶液洗涤晶体,故答案为:酒精(或饱和硫酸锌溶液);
(4)还原除杂工序加入锌粉,可以还原Cd2+为金属Cd,从而除去Cd,发生反应的离子方程式为Zn+Cd2+= Zn2++Cd;根据Cd2+、Zn2+沉淀的pH可知,若直接在“氧化除杂”步骤中除去Cd2+,溶液的pH至少需要调节为9.4,此时Zn2+也会完全沉淀,因此需要在“还原除杂”步骤中除去Cd2+,故答案为:Zn+Cd2+= Zn2++Cd;在氧化除杂工序中加ZnO是为了调节溶液pH,若要完全除去Cd2+,溶液的pH至少需要调节为9.4,此时Zn2+也会完全沉淀;
(5)电池工作时,正极NiO(OH)转化为Ni(OH)2,则放电时,正极反应式为:NiO(OH)+H2O+ e- = Ni(OH)2 +OH-,充电时,阳极发生的反应为放电时正极反应的逆过程,则阳极反应式为:Ni(OH)2-e- +OH- = NiO(OH)+H2O;电解硫酸锌溶液制备锌单质时,阴极锌离子得电子析出金属锌,阳极为水电离出的氢氧根离子放电,电极反应式为:2H2O-4e- =O2↑+4H+,则电解后溶液生成稀硫酸,所以沉积锌后的电解液可返回酸浸工序继续使用,故答案为:Ni(OH)2-e- +OH- = NiO(OH)+H2O;酸浸;
(6)已知酸浸液中砷元素以AsO33-存在,在氧化除杂时加入酸性KMnO4溶液,KMnO4可与AsO33-发生反应生成FeAsO4,As的化合价根据得失电子守恒,电荷守恒、元素守恒,写出该反应的离子方程式为5Fe2+ + 5AsO33- +3MnO4- + 14H+ = 3Mn2+ +5FeAsO4↓+7H2O,故答案为:5Fe2+ + 5AsO33- +3MnO4- + 14H+ = 3Mn2+ +5FeAsO4↓+7H2O。

【题目】氮元素是一种重要的非金属元素,可形成多种化合物。试回答下列有关问题:
(1)①已知4CO(g)+2NO2(g)4CO2(g)+N2(g) △H=-1200kJmol-1。对于该反应,改变某一反应条件,(已知温度T2>T1)下列图象如图1正确的是___(填代号)。

②已知CO与H2O在一定条件下可以发生反应:CO(g)+H2O(g)CO2(g)+H2(g) △H=-QkJmol-1。820℃时,在甲、乙两个恒容密闭容器中,起始时按照下表进行投料,经过一段时间后达到平衡状态,若甲中CO的转化率为40%,则该反应的平衡常数为___;乙容器吸收的热量为___。
甲 | 乙 |
0.10molH2O | 0.20molH2 |
0.10molCO | 0.20molCO2 |
(2)氨水常用作沉淀剂,已知25℃时,Ksp[Fe(OH)3]=2.6×10-39,Ksp[Al(OH)3]=1.1×10-33,向浓度均为0.1molL-1的FeCl3和AlCl3混合溶液中加入氨水,首先生成的沉淀是___(填化学式)。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气,已知:
①N2(g)+2O2(g)=N2O4(l) △H=-19.5kJmol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-534.2kJmol-1
写出肼与四氧化二氮反应的热化学方程式___。
(4)纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL0.1molL-1NaOH溶液中加入0.2molL-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图2。

①根据图象写出HN3的电离方程式:___。
②下列说法正确的是___(填序号)。
A.若用已知浓度的NaOH溶液滴定HN3溶液来测定HN3的浓度时应用甲基橙作指示剂
B.常温下,向0.2molL-1HN3的溶液中加水稀释,则![]() 不变
不变
C.分别中和pH均为4的HN3溶液和HCl溶液,消耗0.1molL-1NaOH溶液的体积相同
D.D点时溶液中离子浓度存在如下关系:2c(H+)+c(HN3)=c(N3-)+2c(OH-)