题目内容
【题目】新型NaBH4/H2O2燃料电池(DBFC)的装置示意图如下,下列叙述正确的是
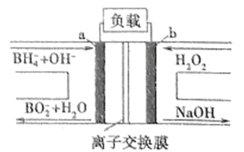
A.b极为正极,发生氧化反应
B.电池应选用阴离子交换膜
C.电子移动方向:电极a→离子交换膜→电极b
D.a极的电极反应式为![]() +8OH--8e-=
+8OH--8e-=![]() +6H2O
+6H2O
【答案】D
【解析】
A.通过分析图中b极是H2O2流入,出来NaOH,说明H2O2转化为了OH-,化合价降低,发还原反应,故b为正极,发生还原反应,A错误;
B.放电时,阳离子向正极移动、阴离子向负极移动,所以Na+从负极区向正极区迁移,故电池应选用阳离子交换膜,B错误;
C.电子移动方向:电极a→导线→电极b,电子只能在导线和电极中移动,不可能在电解质溶液和离子交换膜中移动,C错误;
D.根据元素化合价变化知,负极上BH4-失电子发生氧化反应,a极的电极反应式为BH4-+8OH--8e-=BO2-+6H2O,D正确;
故答案为:D。

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
(1)该反应的化学方程式为 ________________________________
(2)从开始至2min,Z的平均反应速率为 ________________
(3)某探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气 所需时间/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
①该实验的目的是探究 ____________ 、 _______ 对锌和稀盐酸反应速率的影响;
②实验Ⅰ和Ⅱ表明 _________________ ,化学反应速率越大。