题目内容
10.下列各组中的性质比较,正确的是( )①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③还原性:F->Cl->Br-
④稳定性:HCl>H2S>PH3.
| A. | 都正确 | B. | ①②③ | C. | ②③④ | D. | ①②④ |
分析 ①元素的非金属性越强,其最高价氧化物的水化物酸性越强;
②元素的金属性越强,其最高价氧化物的水化物碱性越强;
③元素的非金属性越强,其简单阴离子的还原性越弱;
④元素的非金属性越强,其氢化物的稳定性越强.
解答 解:①元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Cl>Br>I,所以酸性:HClO4>HBrO4>HIO4,故正确;
②元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性Ba>Ca>Mg,所以碱性Ba(OH)2>Ca(OH)2>Mg(OH)2,故正确;
③元素的非金属性越强,其简单阴离子的还原性越弱,非金属性F>Cl>Br,所以还原性:F-<Cl-<Br-,故错误;
④元素的非金属性越强,其氢化物的稳定性越强,非金属性Cl>S>P,所以氢化物的稳定性:HCl>H2S>PH3,故正确;
故选D.
点评 本题考查同一主族、同一周期元素性质递变规律,侧重考查学生分析判断及知识运用能力,以第三周期、第IA族、第VIIA族为例熟悉元素周期律,题目难度不大.

练习册系列答案
相关题目
20.下列各组物质不属于同分异构体的是( )
| A. | 乙醇与甲醚 | B. | 麦芽糖与纤维二糖 | ||
| C. | 淀粉与纤维素 | D. | 2-甲基丁烷和戊烷 |
1.下列各有机物的命名正确的是( )
| A. | 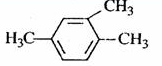 1,3,4-三甲苯 | B. | 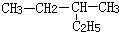 2-乙基丁烷 2-乙基丁烷 | ||
| C. | 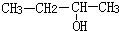 3-丁醇 3-丁醇 | D. | 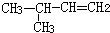 3-甲基-1-丁烯 3-甲基-1-丁烯 |
15.利用相似相溶原理不能解释的是( )
| A. | I2微溶于水,易溶于CCl4;HCl易溶于水 | |
| B. | 在水中的溶解度:C2H5OH>CH3CH2CH2CH2OH | |
| C. | 不同的烃之间相互溶解 | |
| D. | I2易溶于KI溶液中 |
2.钾长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8,其中只有W显负价.X、Y的最外层电子数之和与Z的最高正价数相等,Y3+与W的阴离子具有相同的电子层结构,X、W的质子数之和等于Y、Z的质子数之和.下列说法错误的是( )
| A. | X的离子半径>Y的离子半径 | |
| B. | Z的氢化物稳定性>W的氢化物稳定性 | |
| C. | 化合物X2W2和Y2W3中都不含配位键 | |
| D. | 1 mol ZW2晶体所含Z-W键的数目为4NA |
13.下列关于浓HNO3和浓H2SO4的叙述中正确的是( )
| A. | 由于浓HNO3和浓H2SO4氧化性均较强,常温下都不可用铝制容器贮存 | |
| B. | 露置在空气中,容器内酸液的质量都减轻 | |
| C. | 常温下都能与铜较快反应 | |
| D. | 露置在空气中,容器内酸液的浓度都减小 |