题目内容
【题目】2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。
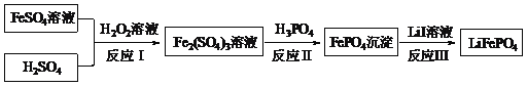
下列说法正确的是( )
A.过氧化氢的电子式为:![]()
B.反应Ⅰ的离子方程式为:2Fe2++H2O2=2Fe3++2OH-
C.反应Ⅱ的离子方程式为:Fe3++PO![]() =FePO4↓
=FePO4↓
D.反应Ⅲ的化学方程可能为:2FePO4+2LiI=2LiFePO4+I2
【答案】D
【解析】
根据工艺流程,硫酸亚铁被过氧化氢在酸性条件下氧化生成硫酸铁,硫酸铁与磷酸反应生成磷酸铁沉淀,磷酸铁与碘化锂发生氧化还原反应得到磷酸亚铁锂,据此分析。
A.过氧化氢为共价化合物,电子式为![]() ,A错误;
,A错误;
B.反应Ⅰ为酸性条件下过氧化氢与亚铁离子反应,反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,B错误;
C.磷酸为弱电解质,书写离子方程式时不能拆开,故反应Ⅱ的离子方程式为Fe3++H3PO4=FePO4↓+3H+,C错误;
D.反应Ⅲ中Fe3+被还原为Fe2+,I-被氧化为I2,根据化合价升降法写出反应的化学方程式为2FePO4+2LiI=2LiFePO4+I2,D正确;
故选D。

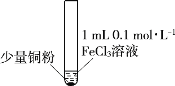
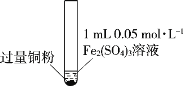
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去, 变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是( )
A.实验I、II、III中均发生了反应2Fe3++Cu=2Fe2++Cu2+
B.对比实验I、II、III说明白色沉淀的产生可能与铜粉的量及溶液的阴离子种类有关
C.实验I、III中加入蒸馏水后c(Cu2+)相同
D.向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀