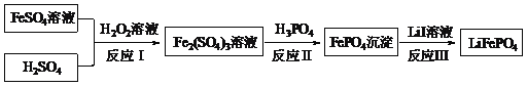��Ŀ����
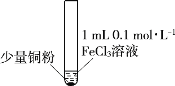
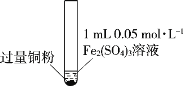
����Ŀ��ijС��ͬѧͨ��ʵ���о�FeCl3��Һ��Cu�۷�����������ԭ��Ӧ��ʵ���¼���£�
��� | I | II | III |
ʵ�鲽�� |
�������2mL����ˮ |
���������2mL����ˮ |
���������2mL����ˮ |
ʵ������ | ͭ����ʧ����Һ��ɫ��dz����������ˮ������������ | ͭ����ʣ�࣬��Һ��ɫ��ȥ����������ˮ�����ɰ�ɫ���� | ͭ����ʣ�࣬��Һ��ɫ��ȥ�� �����ɫ����������ˮ���ް�ɫ���� |
����˵������ȷ���ǣ� ��
A.ʵ��I��II��III�о������˷�Ӧ2Fe3++Cu=2Fe2++Cu2+
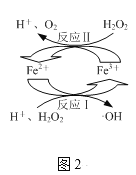
B.�Ա�ʵ��I��II��III˵����ɫ�����IJ���������ͭ�۵�������Һ�������������й�
C.ʵ��I��III�м�������ˮ��c(Cu2+)��ͬ
D.��ʵ��III��Ӧ�����Һ�м��뱥��NaCl��Һ���ܳ��ְ�ɫ����
���𰸡�C
��������
A������ʵ������Һ�о�����Fe3+��������ͭ�ۣ����ᷢ��2Fe3++Cu=2Fe2++Cu2+����A��ȷ��
B���Ա�ʵ��I������֪����ɫ�����IJ�����ͭ�۵����йأ��Ա�ʵ������III��֪����ɫ�����IJ�������Һ�������������йأ���B��ȷ��
C��ʵ��I��ͭ������������ȫ��ʧ�����Բ���ȷ���Ƿ�Fe3+ȫ����Ӧ������ʵ��I��III�м�������ˮ��c(Cu2+)��һ����ͬ����C����
D������ʵ�����������֪����ͭ�����������Ӵ���ʱ�����������������ʵ������Ӧ�����Һ�м��뱥��NaCl��Һ�����ܳ��ְ�ɫ��������D��ȷ��
�ʴ�ΪC��

 ��һ������ĩ�ٷֳ�̾�ϵ�д�
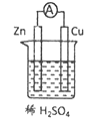
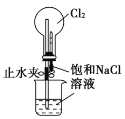
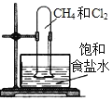
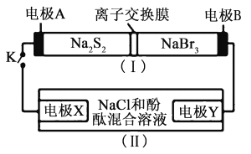
��һ������ĩ�ٷֳ�̾�ϵ�д�����Ŀ����������װ�û��������ʵ�飬���ܴﵽĿ�ĵ��ǣ� ��
|
|
|
���ڹ����� |
A.��ϡ������Cu��Ӧ��ȡNO | B.��֤������ԭ��Ӧ���е���ת�� | C.������Ȫʵ�� | D.��֤����������ܷ�����Ӧ |
A.AB.BC.CD.D
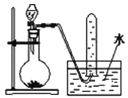
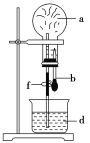
����Ŀ������ͼ��ʾ��װ���У���ƿ�г�����������a�����ι��е�Һ��b������ƿ�ڣ���������ƿ��Ȼ����ɼ�f���ձ��е�Һ��d����Ȫ״��������ռ���������ƿ����a��b�ֱ���(����)
ѡ�� | a(��������) | b(Һ��) |
|
A | NO2 | ˮ | |
B | CO2 | ����NaHCO3��Һ | |
C | Cl2 | ����NaCl��Һ | |
D | NH3 | 1 mol��L��1���� |
A. AB. BC. CD. D