题目内容
【题目】氯胺是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍,下列有关氯胺(NH2Cl)的说法一定不正确的是( )
A.氯胺的水解产物为NH2OH(羟氨)和HCl
B.氯胺的电子式为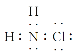
C.氯胺中氯的化合价为+1价
D.氯胺的消毒原理与漂白粉相似
【答案】A
【解析】
试题分析:A、NH2OH(羟氨)和HCl没有强氧化性,由于NH2Cl有强氧化性,所以氯胺的水解可看作NH2-Cl和HO-H互相交换形成NH3和ClOH,将ClOH改写为HClO,故A错误;B、氮原子与氢原子、氯原子之间形成1对共用电子对,电子式为![]() ,故B正确;C、由于氯胺(NH2Cl)有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍,氯元素化合价显正价,H为+1,N为-3价,根据化合价规则可知,NH2Cl中氯元素的化合价为+1价,故C正确;D、氯胺(NH2Cl)有强氧化性,NH2Cl的消毒原理与漂白粉相似,故D正确;故选A。
,故B正确;C、由于氯胺(NH2Cl)有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍,氯元素化合价显正价,H为+1,N为-3价,根据化合价规则可知,NH2Cl中氯元素的化合价为+1价,故C正确;D、氯胺(NH2Cl)有强氧化性,NH2Cl的消毒原理与漂白粉相似,故D正确;故选A。

【题目】有机物A的相对分子质量不超过150, 经测定A具有下列性质:
A的性质 | 推断A的组成、结构 |
①能燃烧,燃烧产物只有CO2和H2O | __________ |
②A与醇或羧酸在浓硫酸存在下均能生成有香味的物质 | __________ |
③在一定条件下,A能发生分子内脱水反应,其生成物与溴水混合,溴水褪色 | |
④0.1 mol A与足量NaHCO3溶液反应产生4.48 L(标准状况下)气体 | ___________ |
(1)填写表中空白。
(2)若A分子中氧元素的质量分数为59.7%,则A的分子式为_______________
(3)若A分子中无含碳支链,写出反应③的化学方程式:_____________________。
(4)下列物质与A互为同系物的是________(填字母)。
a. ![]() b.
b. ![]()
c. ![]() d.
d. ![]()