题目内容
1.如图为某原电池的示意图,则下列有关说法中正确的是( )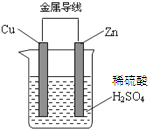
| A. | 锌片是正极 | |
| B. | 铜片上发生的反应为 Cu-2e-═Cu2+ | |
| C. | 电子由铜片通过导线流向锌片 | |
| D. | 该装置能够将化学能转化为电能 |
分析 该装置中,锌易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流向正极.
解答 解:A.锌失电子发生氧化反应而作负极,故A错误;
B.铜作正极,发生的反应为 2H++2e-═H2,故B错误;
C.电子从负极锌沿导线流向正极铜,故C错误;
D.该装置中锌易失电子作负极,铜作正极,为原电池装置,是将化学能转变成电能,故D正确;
故选D.
点评 本题考查了原电池原理,根据电极上得失电子判断正负极,再结合电极反应类型、电子流向来分析解答,熟记原电池原理,难点是电极反应式的书写.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
11.E和F加入密闭容器中,在一定条件下发生反应:E(s)+4F(g)?G(g),已知该反应的平衡常数值如下表所示.下列说法正确的是( )
| 温度℃ | 25 | 80 | 230 |
| 平衡常数值 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述反应是熵增反应 | |
| B. | 25℃时,反应G(g)?E(s)+4F(g)的平衡常数值是0.5 | |
| C. | 在80℃时,测得某时刻,F、G浓度均为0.5 mol•L-1,则此时v(正)<v(逆) | |
| D. | 恒温恒容下,向容器中再充入少量G(g),达新平衡时,F的体积百分含量将增大 |
12.下列分子中所有原子一定处于同一平面的是( )
| A. | CH3CH2CH=CH2 | B. | CH4 | C. | C6H5-C≡CH | D. | CH3CH=CH2 |
9.下列物质之间的相互关系错误的是( )
| A. | H和D互为同位素 | B. |  与 与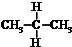 互为同分异构体 互为同分异构体 | ||
| C. | CH3CH3和CH3CH2CH3互为同系物 | D. | O2和O3互为同素异形体 |
16.下列有关化学与自然资源的开发利用说法中不正确的是( )
| A. | 海水提溴是将海水中的化合态的溴富集再转化为游离态的溴 | |
| B. | 石油裂化的主要目的是提高汽油的产量 | |
| C. | 煤干馏的产品很多,是一个化学变化 | |
| D. | 海水提镁的过程为:MgCl2(aq)$\stackrel{石灰乳}{→}$ Mg(OH)2$\stackrel{煅烧}{→}$MgO$\stackrel{电解}{→}$Mg |
6.下列表示对应化学反应的离子方程式正确的是( )
| A. | 漂白粉露置在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 向滴有酚酞的硅酸钠溶液中边加边振荡地滴加盐酸至红色变浅并接近消失:2H++SiO32-═H2SiO3(胶体) | |
| C. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O═2SO32-+4Cl-+6H+ | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3═FeO42-+3Cl-+H2O+4H+ |
17.下列分子中的α键是由两个原子的p轨道以“头碰头”方式重叠构建而成的是( )
| A. | CCl4 | B. | Cl2 | C. | H2 | D. | HF |
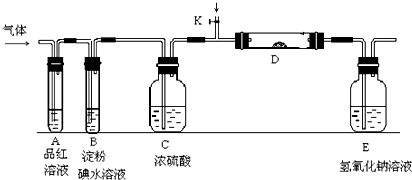
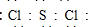 ,Y2W2的结构式为Cl-S-S-Cl.
,Y2W2的结构式为Cl-S-S-Cl.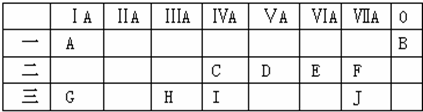
 ,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.
,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.