题目内容
8.下列物质中,所含化学键类型完全相同的是( )| A. | CaCl2 K2S | B. | CO2 Na2O2 | C. | NaOH HCl | D. | NH4Cl CaH2 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,部分碱、大多数盐及金属氧化物、铵盐中含有离子键,据此分析解答.
解答 解:A.这两种物质中都只含离子键,化学键类型相同,故A正确;
B.二氧化碳分子中C-O原子之间只存在共价键,过氧化钠中钠离子和过氧根离子之间存在离子键、O-O原子之间存在共价键,所以化学键类型不同,故B错误;
C.NaOH中钠离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,HCl分子中H-Cl原子之间只存在共价键,所以化学键类型不同,故C错误;
D.氯化铵中铵根离子和氯离子之间存在离子键、铵根离子中N-H原子之间存在共价键,氢化钙中钙离子和氢离子之间只存在离子键,所以化学键类型不同,故D错误;
故选A.
点评 本题考查化学键判断,侧重考查基本概念,明确离子键和共价键的区别是解本题关键,注意氢化钙属于离子化合物,为易错点.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
18.乙醇分子中不同的化学键如图所示,下列不同反应中键的断裂不正确的是( )
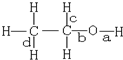

| A. | 和乙酸发生酯化反应键a断裂 | |
| B. | 和氢溴酸反应键a断裂 | |
| C. | 在铜催化和加热条件下和氧气反应键a、c断裂 | |
| D. | 和浓硫酸共热至170℃时键b和d断裂 |
16.已知A、B、C、D、E、F六种元素的原子序数依次递增,前四种元素为短周期元素.A位于元素周期表s区,基态原子中电子层数与未成对电子数相等;B基态原子中电子占据三种能量不同的原子轨道,且每种能量不同的原子轨道中的电子数相同;C基态原子核外成对电子数为未成对电子数的3倍;D与C同主族;E、F位于同一周期和同一族,且E比F的核电荷数小2.
(1)E3+的核外有5个未成对电子,A2C2的电子式为 .
.
(2)F(BC)n的中心原子价电子数与配体提供电子总数之和为18,则n=4.
(3)B的一种氢化物分子中共有14个价电子,该分子中存在的共价键类型有ABFG.(填代号)
A.非极性键 B.极性键 C. s-sσ键 D.s-pσ键
E.p-pπ键 F.s-sp3σ键 G.sp3-sp3σ键H.sp3-sp3 π键
(4)A2D和A2C2的主要物理性质比较如下:
A2D和A2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因H2O2分子之间有氢键,而H2S分子间不存在氢键,所以H2O2的熔沸点比H2S高,H2O2与水分子之间能形成氢键,所以H2O2易溶于水,而H2S不能,所以H2O2在水中的溶解性比H2S好.
(1)E3+的核外有5个未成对电子,A2C2的电子式为
 .
.(2)F(BC)n的中心原子价电子数与配体提供电子总数之和为18,则n=4.
(3)B的一种氢化物分子中共有14个价电子,该分子中存在的共价键类型有ABFG.(填代号)
A.非极性键 B.极性键 C. s-sσ键 D.s-pσ键
E.p-pπ键 F.s-sp3σ键 G.sp3-sp3σ键H.sp3-sp3 π键
(4)A2D和A2C2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| A2D | 187 | 202 | 2.6 |
| A2C2 | 272 | 423 | 以任意比互溶 |
3.有A、B、C、D四块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,外电路电流由D到C;
③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.
据此,判断四种金属的活动性顺序是( )
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,外电路电流由D到C;
③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.
据此,判断四种金属的活动性顺序是( )
| A. | A>C>D>B | B. | A>B>C>D | C. | C>A>D>B | D. | C>B>D>A |
13.已知阴离子X n-含有N个中子,元素X的质量数为A,则a g Xn- 中含电子的物质的量是( )
| A. | $\frac{A-N-n}{aA}$ mol | B. | $\frac{a(A-N)}{A}$ mol | C. | $\frac{m(A-N-n)}{A}$ mol | D. | $\frac{a(A-N+n)}{A}$ mol |
20.一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相同,将 1.0L这种混合气体在氧气中充分燃烧,生成2.0LCO2和2.4L水蒸气(相同条件下测定).则混合物中烷烃和烯烃的体积比为( )
| A. | 3:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
17. (1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:
(1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:
$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
该反应的平衡常数表达式K=$\frac{[C{O}_{2}]}{[CO]}$,△H<0(填“>”、“<”或“=”);
(2)工业上CO 也用于合成甲醇:
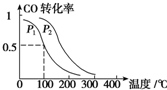
CO(g)+2H2(g)?CH3OH(g)△H=-90.1kJ•mol-1.一定压强下,向容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.
①p1小于p2(填“大于”、“小于”或“等于”);
②100℃时,该反应的化学平衡常数K=$(\frac{V}{a})^{2}$(mol•L-1)-2;
③保持其它条件不变,下列措施中能够增大上述合成甲醇反应的反应速率、且能提高CO转化率的是cd.(填字母).
a.使用高效催化剂 b.降低反应温度 c.通入H2d.再增加a mol CO和2a molH2 e.不断将CH3OH从反应混合物中分离出来.
 (1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:
(1)CO是高炉炼铁的主要反应物之一,发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)工业上CO 也用于合成甲醇:
CO(g)+2H2(g)?CH3OH(g)△H=-90.1kJ•mol-1.一定压强下,向容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.
①p1小于p2(填“大于”、“小于”或“等于”);
②100℃时,该反应的化学平衡常数K=$(\frac{V}{a})^{2}$(mol•L-1)-2;
③保持其它条件不变,下列措施中能够增大上述合成甲醇反应的反应速率、且能提高CO转化率的是cd.(填字母).
a.使用高效催化剂 b.降低反应温度 c.通入H2d.再增加a mol CO和2a molH2 e.不断将CH3OH从反应混合物中分离出来.
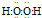 .
.