题目内容
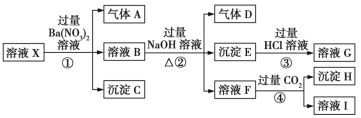
【题目】某强酸性溶液X:可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,转化关系如图所示。反应过程中有一种气体在空气中会变为红棕色。回答下列问题:
(1)沉淀C是___(填化学式),由此可确定溶液X中肯定不存在的阳离子有___。
(2)气体A是___(填化学式),产生气体A的离子方程式为___。
(3)步骤④中发生反应的离子方程式为___。
(4)根据题给信息和图中转化关系,可以确定溶液X中肯定存在的离子有___,可能存在的离子有___。
【答案】BaSO4 Ba2+ NO 3Fe2++4H++NO3-=3Fe3++NO↑+2H2O AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- Al3+、NH4+、SO42-、Fe2+ Fe3+
【解析】
①溶液X为强酸性,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液X和硝酸钡溶液反应生成沉淀C,则溶液X中存在SO42-,不存在和硫酸根离子反应的Ba2+,沉淀C是BaSO4;
②酸性条件下硝酸根离子具有强氧化性,溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,在空气中会变为红棕色,则溶液中存在Fe2+、不存在NO3-,气体A是NO;
③溶液B中加入氢氧化钠溶液、加热时,产生气体D,则溶液中含有NH4+,D是NH3,产生沉淀E,则E中含有Fe(OH)2,可能含有Fe(OH)3;
④溶液F中通入过量CO2生成沉淀H,则溶液X中含有Al3+;
综上,强酸性溶液X中:溶液X中肯定不存在的离子有CO32-、SiO32-、NO3-、Ba2+,肯定存在的离子有Al3+、NH4+、Fe2+、SO42-,可能存在的离子为Fe3+。
(1)溶液X为强酸性,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液X和硝酸钡溶液反应生成沉淀C,则溶液X中存在SO42-,不存在和硫酸根离子反应的Ba2+,沉淀C是BaSO4;
(2)酸性条件下硝酸根离子具有强氧化性,加入硝酸钡产生气体,在空气中会变为红棕色,则溶液中存在Fe2+、不存在NO3-,气体A是NO,反应的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(3)溶液F中通入过量CO2生成沉淀H,步骤④中发生反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。
(4)根据题给信息和图中转化关系,强酸性溶液X中:溶液X中肯定不存在的离子有CO32-、SiO32-、NO3-、Ba2+,肯定存在的离子有Al3+、NH4+、Fe2+、SO42-,可能存在的离子为Fe3+。

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案【题目】对于元素周期表中下列位置的①~⑩10种元素,请用元素符号或化学式回答有关问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ① | ② | ||||||
二 | ③ | ④ | ⑤ | ⑥ | ||||
三 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑦在元素周期表中的位置____________。
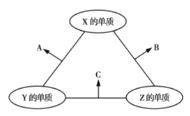
(2)以上元素所形成的最高价含氧酸酸性最强的酸是____________,(填化学式,下同)碱性最强的碱是____________。它们与⑨的单质反应的离子方程式分别为____________、____________。
(3)④⑤⑥的原子半径的由大到小顺序为____________。(填元素符号)③④⑤⑥的最简单氢化物的稳定性由弱到强的顺序为____________。
(4)⑤⑦的一种1:1型化合物X的电子式为____________。X能和①⑤组成的一种化合物Y反应生成⑤的单子,则化学方程式为____________。
【题目】已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/c2(CH3OH),该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题:
(1)写出上述反应的化学方程式:_________________________________ 。
(2)该反应的△H _________0。
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL-1) | 0.54 | 0.68 | 0.68 |
①此时温度400℃,则某时刻υ正_______υ逆(填<、>或=,下同)。
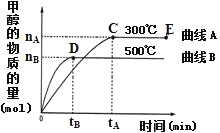
②若以温度为横坐标,以该温度下平衡态甲醇物质的量n为纵坐标,此时反应点在图象的位置是图中____点,比较图中B、D两点所对应的正反应速率υB_______υD,理由是____。

(4)一定条件下要提高反应物的转化率,可以采用的措施是___________。
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物