题目内容
【题目】研究CO2的综合利用对促进“低碳经济”的发展有重要意义。
(1)工业上以CO2、NH3为原料生产尿素[CO(NH2)2],反应实际为两步进行:
I:2NH3(g)+CO2(g)![]() H2NCOONH4(s) △H1=-272kJ·mol-1
H2NCOONH4(s) △H1=-272kJ·mol-1
II:H2NCOONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+138kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+138kJ·mol-1
已知:H2O(l)==H2O(g) △H3=+44kJ·mol-1
①请写出以NH3、CO2为原料,合成尿素和液态水的热化学方程式______________。
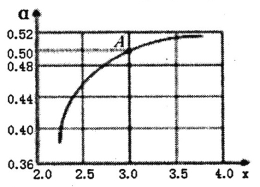
②T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,如图是CO2平衡转化率(![]() )与x的关系。求图中A点NH3的平衡转化率
)与x的关系。求图中A点NH3的平衡转化率![]() =________%。
=________%。
③当x=1.0时,若起始的压强为p0kPa,水为液态,平衡时压强变为起始的1/2。则该反应的平衡常数Kp=_______(kPa)-3(KP为以分压表示的平衡常数)。
(2)用CO2和H2合成甲醇:3H2(g)+CO2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下:
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下:
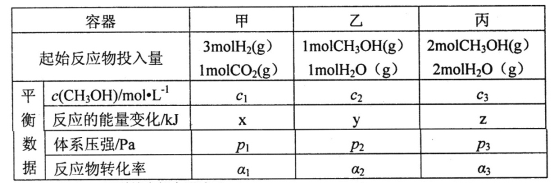
①甲容器10s达到平衡时测得x=39.2,则甲中CO2的平均反应速率____________。
②下列说法正确的是________(填字母编号)。
A.2c1<c3 B.z<2y C.p3>2p2 D.α1+α3>1
(3)用NaOH溶液做碳捕捉剂可获得化工产品Na2CO3。常温下若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=_____[K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11],溶液中c(Na+)_____c(HCO3-)+2c(CO32-)(填“>”“=”或“<”)。
【答案】2NH3(g)+CO2(g)H2O(l)+CO(NH2)2(s) ΔH=-178 kJmol-1 33.3 Kp=108/p03 0.04 molL-1s-1 AB 1︰2或0.5 >
【解析】
本题研究CO2的综合利用对促进“低碳经济”的发展有重要意义,实际以CO2的性质为载体考查了化学反应原理的综合知识,难度适中。
(1) ①NH3、CO2为原料,合成尿素和液态水的热化学方程式为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l) △H,根据盖斯定律可知△H=△H1+△H2-△H3=-178 kJmol-1,因而有2NH3(g)+CO2(g)H2O(l)+CO(NH2)2(s) ΔH=-178 kJmol-1;
CO(NH2)2(s)+H2O(l) △H,根据盖斯定律可知△H=△H1+△H2-△H3=-178 kJmol-1,因而有2NH3(g)+CO2(g)H2O(l)+CO(NH2)2(s) ΔH=-178 kJmol-1;
②A点时,n(NH3)/n(CO2)=3.0,设n(CO2)=1mol,n(NH3)=3mol,CO2平衡转化率为0.50,则转化的CO2的量为1mol×0.50=0.5mol,那么根据2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)可知转化的NH3为0.5mol×2=1mol,NH3的平衡转化率
CO(NH2)2(s)+H2O(l)可知转化的NH3为0.5mol×2=1mol,NH3的平衡转化率![]() =1mol/3mol×100%=33.3%;
=1mol/3mol×100%=33.3%;
③当x=1.0时,设n(NH3)=n(CO2)=1mol,根据三段式可知:
2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)
CO(NH2)2(s)+H2O(l)
起 1 1
转 2x x
平 1-2x 1-x
又若起始的压强为p0kPa,水为液态,平衡时压强变为起始的1/2,可知![]() =
=![]() ,解得x=
,解得x=![]() mol,则n平(NH3)=
mol,则n平(NH3)=![]() mol,n平(CO2)=
mol,n平(CO2)=![]() mol,那么p平(NH3)=
mol,那么p平(NH3)=![]() ×
×![]() =
=![]() kPa,p平(CO2)=
kPa,p平(CO2)= ![]() ×
×![]() =
=![]() kPa,因而Kp=
kPa,因而Kp=![]() =
=![]() (kPa)-3;
(kPa)-3;
(2)①根据3H2(g)+CO2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1,可知消耗的CO2的量为1mol×
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1,可知消耗的CO2的量为1mol×![]() =0.8mol,v(CO2)=
=0.8mol,v(CO2)=![]() =0.04mol·L-1·s-1;
=0.04mol·L-1·s-1;
②A.已知甲和乙为全等等效平衡,平衡时c1=c2,乙和丙的投料比相等,若处于恒压时,c2=c3*,c3*为恒压时丙中甲醇浓度,此时,丙是乙体积的两倍,但题目要求恒容,因而可将丙压缩一半体积,瞬间浓度为2c3*,由于压缩体积相当于加压,根据气体计量数可知,平衡向右移动,则甲醇浓度变大,因而c3>2c3*,综合上述分析可知c3>2c1,A正确;
B.乙和丙的投料比相等,假设在恒压时,c2=c3*,c3*为恒压时丙中甲醇浓度,由于丙是乙体积的两倍,丙中甲醇的消耗量是乙的两倍,可推出吸收的热量关系为z*=2y(注意乙和丙为逆反应,为吸热反应),z*为恒压时丙中热量变化,但题目要求恒容,因而可将丙压缩一半体积,由于压缩体积相当于加压,根据气体计量数可知,平衡向右移动,则甲醇的量变多,即吸收的热量减少,即z< z*,故z<2y,B正确;
C.根据B中分析可知平衡时,丙中甲醇的消耗量是小于乙中甲醇的消耗量的两倍,由于恒温恒容时压强之比等于物质的量之比,因而可推知丙中气体压强是小于乙中气体的两倍,即p3<2p2,C错误;
D.已知甲和乙为全等等效平衡,平衡时c1=c2,甲中α1=2c1/1=2c1,乙中α2=(1-2c2)/1=1-2c2,因而α1+α2=2c1+1-2c2=1,根据C可知平衡时,丙中甲醇的消耗量是小于乙中甲醇的消耗量的两倍,因而α3小于α2,所以α1+α3<1,D错误。
故答案选AB。
(3) pH=10,c(H+)=10-10mol/L,又K2(H2CO3)=![]() ,因而c(CO32-):c(HCO3-)= K2(H2CO3)/c(H+)=1︰2,溶液中电荷守恒关系式为c(Na+)+ c(H+)=c(HCO3-)+2c(CO32-)+ c(OH-),又溶液pH=10,则c(OH-)> c(H+),所以c(Na+)>c(HCO3-)+2c(CO32-)。
,因而c(CO32-):c(HCO3-)= K2(H2CO3)/c(H+)=1︰2,溶液中电荷守恒关系式为c(Na+)+ c(H+)=c(HCO3-)+2c(CO32-)+ c(OH-),又溶液pH=10,则c(OH-)> c(H+),所以c(Na+)>c(HCO3-)+2c(CO32-)。

 通城学典默写能手系列答案
通城学典默写能手系列答案