ЬтФПФкШн
ЁОЬтФПЁПвбжЊГЃЮТЯТ,Ka1(H2CO3)=4.3ЁС10-7,Ka2(H2CO3)=5.6ЁС10-11ЁЃФГЖўдЊЫсH2RМАЦфФЦбЮЕФШмвКжа,H2RЁЂHR-ЁЂR2-Ш§епЕФЮяжЪЕФСПЗжЪ§ЫцШмвКpHБфЛЏЙиЯЕШчЭМЫљЪОЃЌЯТСаа№ЪіДэЮѓЕФЪЧЃЈ ЃЉ
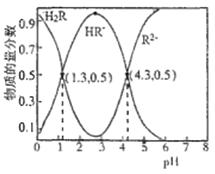
A.дкpH=4.3ЕФШмвКжаЃК3c(R2-)=c(Na+)+c(H+)-c(OH-)
B.ЕШЬхЛ§ЁЂЕШХЈЖШЕФNaOHШмвКгыH2RШмвКЛьКЯКѓЃЌДЫШмвКжаЫЎЕФЕчРыГЬЖШБШДПЫЎаЁ
C.дкpH=3ЕФШмвКжаДцдк![]() =10-3
=10-3
D.ЯђNa2CO3ШмвКжаМгШыЩйСПH2RШмвКЃЌЗЂЩњЗДгІЃКCO32-+H2R=HCO3-+HR-
ЁОД№АИЁПD
ЁОНтЮіЁП
AЃЎОнЭМПЩжЊдкpH=4.3ЕФШмвКжаЃЌc(R2-)=c(HR-)ЃЌШмвКжаЕчКЩЪиКуЮЊЃК2c(R2-)+c(HR-)+c(OH-)=c(Na+)+c(H+)ЃЌЫљвд3c(HR-)=c(Na+)+c(H+)-c(OH-)ЃЌЙЪAе§ШЗЃЛ
BЃЎЕШЬхЛ§ЁЂЕШХЈЖШЕФNaOHШмвКгыH2RШмвКЛьКЯКѓЃЌДЫЪБЗДгІЩњГЩNaHRЃЌОнЭМПЩжЊИУШмвКГЪЫсадЃЌЫЕУїHR-ЕФЕчРыГЬЖШДѓгкHR-ЕФЫЎНтГЬЖШЃЌHR-ЕчРывжжЦЫЎЕФЕчРыЃЌЫљвдДЫШмвКжаЫЎЕФЕчРыГЬЖШБШДПЫЎаЁЃЌЙЪBе§ШЗЃЛ
CЃЎ![]() ЃЌЕБШмвКpH=1.3ЪБЃЌc(H2R)=c(HR-)ЃЌдђKh2=
ЃЌЕБШмвКpH=1.3ЪБЃЌc(H2R)=c(HR-)ЃЌдђKh2=![]() =10-12.7ЃЌШмвКЕФpH=4.3ЪБЃЌc(R2-)=c(HR-)ЃЌдђKa2=
=10-12.7ЃЌШмвКЕФpH=4.3ЪБЃЌc(R2-)=c(HR-)ЃЌдђKa2=![]() =10-4.3ЃЌЫљвд
=10-4.3ЃЌЫљвд ![]() =10-3ЃЌЙЪCе§ШЗЃЛ
=10-3ЃЌЙЪCе§ШЗЃЛ
DЃЎгЩH2RЕФЕчРыГЃЪ§Ka2ДѓгкH2CO3ЕФKa2ЃЌМДЫсадЃКHR-ЃОHCO3-ЃЌЫљвдЯђNa2CO3ШмвКжаМгШыЩйСПH2RШмвКЃЌЗЂЩњЗДгІЃК2CO32-+H2R=2HCO3-+R2-ЃЌЙЪDДэЮѓЃЛ
ЙЪД№АИЮЊDЁЃ