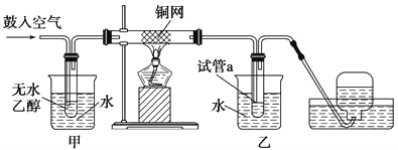
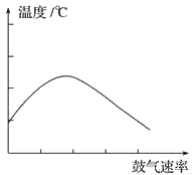
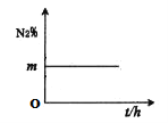
��Ŀ����
����Ŀ��Ŀǰ��﮵������չ������ﮡ�����ﮡ���̼������������﮵ȵ����ϵ����ش��������⣺
��1����̬Niԭ�ӵļ۵����Ų�ʽΪ________����Niͬ�����һ�̬ԭ�Ӻ���ijɵ���������Ni��ͬ��Ԫ�ػ���__________�֡�
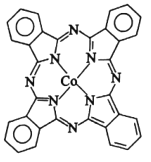
��2��̪ݼ�ܷ��ӵĽṹ��ʽ��ͼ��ʾ����������Ϊ�����ӣ������е�ԭ�ӵ��ӻ�����Ϊ___��
��3��Li�������ѳ�����﮵�ؽṹ̮������O2����ը��ʵ��֤ʵO2����е����Ӷ���Ϊ˳���Է��ӡ����нṹʽ���ڵ�������ӣ������п��ܴ���O2���ӽṹ����__������ĸ����
A ![]() B
B ![]() C
C ![]() D
D ![]()
��4����ͼΪSiO2������Siԭ����z�᷽����xyƽ���ͶӰͼ��������ͶӰͼ��������Oԭ����ȥ��Siԭ���Ա�ע�����ֱ�ʾÿ��Siԭ��λ��z��ĸ߶ȣ���SiA��SiB�ľ�����______��
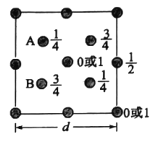
��5��PCl5����ľ�����ͼ��ʾ���þ�������ʱ�γ�һ���ܵ����Һ�壬ʵ�������к���һ���������������Ӻ�һ���������������ӣ���P��Cl���ļ���ֻ��198pm��206pm���֣����õ��뷽��ʽ����PCl5�����ܵ����ԭ��____�������������������м��Ǵ���PCl3�ļ���ԭ��Ϊ_____����֪�þ���ľ����߳�Ϊapm��NAΪ����٤��������ֵ����þ�����ܶ�Ϊ__________g��cm��3��

���𰸡�![]() 3
3 ![]() ��
��![]() B
B ![]()
![]()
![]() ������Pԭ����һ�Թ¶Ե��ӣ�
������Pԭ����һ�Թ¶Ե��ӣ�![]() ��Pû�й¶Ե��ӣ��¶Ե��ӶԳɼ����ӵ��ų������ڳɼ����ӶԼ���ų���
��Pû�й¶Ե��ӣ��¶Ե��ӶԳɼ����ӵ��ų������ڳɼ����ӶԼ���ų��� ![]()
��������
(1)NiԪ��Ϊ28��Ԫ�أ����������Ų�Ϊ1s22s22p63s23p63d84s2������۵����Ų�ʽΪ3d84s2��Niԭ�Ӻ�������е�������2����ͬ���ڵ�����ͬ��2������3��Ԫ�أ��۵����Ų��ֱ�Ϊ3d24s2��4s24p2��4s24p4���ֱ���Ti��Ge��Se����3�֣�
(2)�÷����У�Nԭ�����γ�3���Ҽ�������1�Թ¶Ե��ӣ����γ�4��������û�й¶Ե��ӣ�������Nԭ�ӵ��ӻ����;�Ϊsp3������Nԭ���γ�2������������1�Թ¶Ե��ӣ�����Nԭ�ӵ��ӻ����;�Ϊsp2��
(3)ʵ��֤ʵO2����е����Ӷ���Ϊ˳���Է��ӡ�����ѡ����з�������֪A��C��D�е�O2���ӵĽṹʽ�У���û�е����Ӵ��ڣ���˲�������ʵ��ʵ����Bѡ��O2�Ľṹʽ�еĻ�ѧ����3�����ӣ��е����ӣ����Bʵ����ʵ��
(4)����ͼ ��֪����άģ��Ϊ
��֪����άģ��Ϊ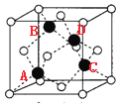 (ͼ�к���Ͱ����Ϊ��ԭ�ӣ���ԭ��λ��������ԭ��֮�䣬ʡ��)��ͼ��ABCD�ĸ�Siԭ���γ���������ṹ����AB�������AC���룬AC�����ڵ���ͶӰΪ������Խ��ߵ�һ�룬��SiA��SiB�ľ���=
(ͼ�к���Ͱ����Ϊ��ԭ�ӣ���ԭ��λ��������ԭ��֮�䣬ʡ��)��ͼ��ABCD�ĸ�Siԭ���γ���������ṹ����AB�������AC���룬AC�����ڵ���ͶӰΪ������Խ��ߵ�һ�룬��SiA��SiB�ľ���=![]() ��
��
(5))���������ƶ����ӵĻ������ܵ��磬PCl5��һ�ְ�ɫ���壬����ʱ�γ�һ���ܵ����Һ�������к���һ�����������������Ӻ�һ�����������������ӣ������ӡ������ӷֱ�ΪPCl4+��PCl6-������뷽��ʽΪ2PCl5=PCl4++PCl6-��PCl3������Pԭ����һ�Թµ��Ӷԣ�PCl4+��Pû�йµ��Ӷԣ��µ��ӶԶԳɼ����ӵ��ų������ڳɼ����ӶԼ���ų��������������������������м��Ǵ���PCl3�ļ��ǣ��þ�����PCl5����=![]() ���������=(a��10-10cm)3�������ܶ�
���������=(a��10-10cm)3�������ܶ�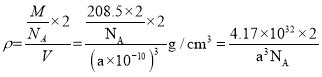 g/cm3��
g/cm3��

 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�