题目内容
【题目】高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
组分 | SiO2 | MgO | Na2O | K2O | Fe2O3 |
质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.8 |
通过下图流程可由蛇纹石制备较纯净的二氧化硅。
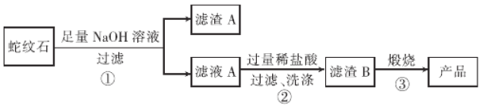
(1)蛇纹石中涉及的可溶性金属氧化物有____________(写化学式)。
(2)步骤①中涉及SiO2反应的离子方程式为________________。
(3)滤渣A 的成分有______________________(填化学式)。
(4)步骤②中洗涤沉淀的方法是_____________________。
(5)步骤③反应的化学方程式为______________________;实验室进行步骤③需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、和________________。
【答案】Na2O、K2O SiO2+2OH-=SiO32-+H2O MgO和Fe2O3 向漏斗中注入蒸馏水至浸没沉淀,让水自然流下,重复操作2至3次 H2SiO3![]() SiO2+H2O 坩埚钳、三脚架
SiO2+H2O 坩埚钳、三脚架
【解析】
蛇纹石(含SiO2、MgO、Na2O、K2O、Fe2O3)加入足量氢氧化钠进行碱浸溶解,SiO2可与氢氧化钠反应生成硅酸钠,Na2O、K2O可与氢氧化钠溶液中的水反应生成氢氧化钠和氢氧化钾;MgO、Fe2O3不与氢氧化钠溶液反应,也不溶于水,则滤渣A为MgO、Fe2O3,滤液A主要含有K+、Na+、OH-、SiO32-,加入过量盐酸中和滤液A中的碱,同时SiO32-在酸性条件下转化为H2SiO3沉淀,经过滤、洗涤,得到滤渣B为H2SiO3,对其煅烧分解生成SiO2,据此分析解答。
(1)根据分析,蛇纹石中含有的可溶性金属氧化物有Na2O和K2O,它们能与水反应生成氢氧化钠和氢氧化钾;
(2)二氧化硅属于酸性氧化物,可与氢氧化钠溶液反应生成硅酸钠和水,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O;
(3)氧化钠与氧化钾属于可溶性氧化物,氧化铝属于两性氧化物,二氧化硅属于酸性氧化物,上述四种物质都能溶解在氢氧化钠溶液中,氧化镁和氧化铁属于碱性氧化物且难溶于水,因此,滤渣A的成分有MgO和Fe2O3;
(4)步骤②生成沉淀的成分是硅酸,洗涤过滤出的沉淀的方法是:向过滤器中注入蒸馏水至浸没沉淀,待水自然流出后,重复上述操作两到三次;
(5)步骤③用灼烧的方法使硅酸分解生成二氧化硅,化学方程式为:H2SiO3![]() SiO2+H2O,实验室灼烧固体时需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、坩埚钳和三脚架。
SiO2+H2O,实验室灼烧固体时需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、坩埚钳和三脚架。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为___________(写离子符号);若所得溶液c(HCO3)∶c(CO32)=2∶1,溶液pH=___________。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=______。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是____(填“A” 或“B ”)。