题目内容
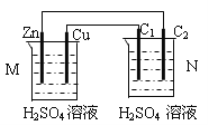
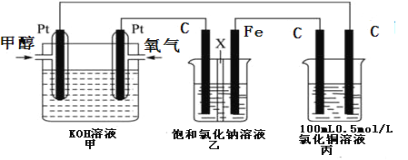
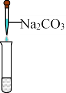
【题目】有关物质的转化关系如下图所示(反应条件已略去)。已知:A为紫红色金属,B是强酸,E能使品红溶液褪色,F是海水的主要成分,H是一种难溶于水的白色固体,摩尔质量为99.5 g·mol-1,I溶液呈黄色,工业上可作为印刷电路板蚀刻液。

请回答下列问题:
(1)H的化学式为_____。
(2)F的电子式为_____。
(3)写出反应①的化学方程式_____。
(4)写出反应③的离子方程式_____。
【答案】CuCl ![]() Cu + 2H2SO4(浓)
Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑ + 2H2O CuCl + Fe3+ = Fe2+ + Cu2+ + Cl-
CuSO4 + SO2↑ + 2H2O CuCl + Fe3+ = Fe2+ + Cu2+ + Cl-
【解析】
A为紫红色金属,则应为Cu,B是强酸,E能使品红溶液褪色,则B是浓硫酸,E为SO2,反应①为Cu与浓硫酸在加热条件下发生反应生成硫酸铜、二氧化硫和水,F是海水的主要成分,F为NaCl,H是一种难溶于水的白色固体,摩尔质量为99.5 g·mol-1,则H应为CuCl,I溶液呈黄色,工业上可作为印刷电路板蚀刻液,则I为FeCl3溶液,以此解答该题。
(1)根据以上分析,H的化学式为CuCl,
因此,本题正确答案是:CuCl;
(2)根据以上分析,F为NaCl,则F的电子式为![]() ,
,
因此,本题正确答案是:![]() ;
;
(3)根据以上分析,反应①为Cu与浓硫酸在加热条件下发生反应生成硫酸铜、二氧化硫和水,则反应的化学方程式Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑ + 2H2O,
CuSO4 + SO2↑ + 2H2O,
因此,本题正确答案是:Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑ + 2H2O ;
CuSO4 + SO2↑ + 2H2O ;
(4)根据以上分析,反应③为氯化亚铜和氯化铁溶液发生的氧化还原反应,反应的离子方程式为:CuCl + Fe3+ = Fe2+ + Cu2+ + Cl-,
因此,本题正确答案是:CuCl + Fe3+ = Fe2+ + Cu2+ + Cl-。

【题目】高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
组分 | SiO2 | MgO | Na2O | K2O | Fe2O3 |
质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.8 |
通过下图流程可由蛇纹石制备较纯净的二氧化硅。
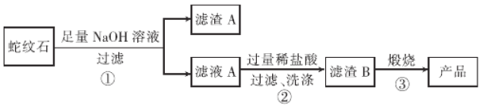
(1)蛇纹石中涉及的可溶性金属氧化物有____________(写化学式)。
(2)步骤①中涉及SiO2反应的离子方程式为________________。
(3)滤渣A 的成分有______________________(填化学式)。
(4)步骤②中洗涤沉淀的方法是_____________________。
(5)步骤③反应的化学方程式为______________________;实验室进行步骤③需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、和________________。