题目内容
【题目】氨气与适量氯气混合反应可生成NH4Cl(岩脑砂的主要成分)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。
A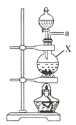 B
B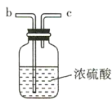
C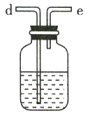 D
D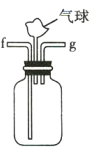
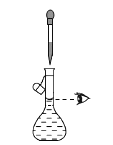
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为 ________________ 。
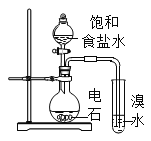
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→ ________________ → ________________ → ________________ → ________________ 。
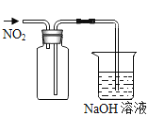
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从__________ 通入,反应的化学方程式为 ___________;可能观察到的现象是________________。
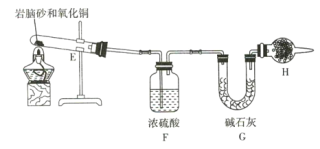
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
①为顺利完成有关物理量的测定,请完善下列表格。
测量时间点 | 反应前 | 反应后 |
测量内容 | ________________ | 当观察到 ________________ 现象时停止加热,冷却,称量H装置的总质量 |
②如果不用H装置,测出NH4Cl的含量将 _____ (填“偏高”“偏低”或“无影响”)。
【答案】圆底烧瓶 d e b c f 8NH3+3Cl2=6NH4Cl+N2 黄绿色气体消失,有白烟生成 称量G的总质量 F中不再有气泡出现 偏高
【解析】
NH4Cl的制备:A由浓盐酸与MnO2制备Cl2,反应为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,制得的氯气混有HCl和水蒸气,依次通过饱和食盐水、浓硫酸除去,为保证除杂充分,导气管均长进短出,得到纯净干燥的氯气,将适量氨气与氯气充分混合反在D中反应:8NH3+3Cl2=6NH4Cl+N2,该反应是个气体体积减少的反应。
Mn2++Cl2↑+2H2O,制得的氯气混有HCl和水蒸气,依次通过饱和食盐水、浓硫酸除去,为保证除杂充分,导气管均长进短出,得到纯净干燥的氯气,将适量氨气与氯气充分混合反在D中反应:8NH3+3Cl2=6NH4Cl+N2,该反应是个气体体积减少的反应。
NH4Cl纯度的测定:E中发生反应2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O,F中浓硫酸吸收生成的水蒸气,同时观察气体的生成,F中无气泡时,说明NH4Cl反应完全,H中的碱石灰吸收生成HCl气体,由HCl气体的质量,根据氯元素守恒或者方程可得NH4Cl的量,H的作用是防止外界的水蒸气和二氧化碳进入G装置被吸收,增大误差,据此分析作答。
3Cu+N2↑+2HCl↑+3H2O,F中浓硫酸吸收生成的水蒸气,同时观察气体的生成,F中无气泡时,说明NH4Cl反应完全,H中的碱石灰吸收生成HCl气体,由HCl气体的质量,根据氯元素守恒或者方程可得NH4Cl的量,H的作用是防止外界的水蒸气和二氧化碳进入G装置被吸收,增大误差,据此分析作答。
(1)装置A中仪器X的名称为圆底烧瓶;
(2)要先用饱和食盐水除去氯气中的HCl气体,再进行干燥,故要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→d→e→b→c;
(3)氨气的密度小, NH3应从f口进,氯气的密度大于氨气的密度,应从g口进,有利于两种气体充分混合,反应的化学方程式为8NH3+3Cl2=6NH4Cl+N2,可能观察到的现象是:黄绿色气体消失,同时有白烟生成;
(4)E中NH4Cl、CuO发生反应产生HCl、N2、Cu、H2O,反应方程式为:2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O,G中浓硫酸将气体干燥,当观察到F中不再有气泡出现时,反应结束;G中碱石灰增重的质量为HCl的质量,故加热前要称量G的总质量。②如果不用H装置,空气中的水和二氧化碳会进入G中,使测出NH4Cl的含量将偏高。
3Cu+N2↑+2HCl↑+3H2O,G中浓硫酸将气体干燥,当观察到F中不再有气泡出现时,反应结束;G中碱石灰增重的质量为HCl的质量,故加热前要称量G的总质量。②如果不用H装置,空气中的水和二氧化碳会进入G中,使测出NH4Cl的含量将偏高。

 阅读快车系列答案
阅读快车系列答案【题目】取体积均为1 L的四组X的溶液进行实验(X受热发生分解反应),在不同温度下测得X的物质的量(mol)随时间的变化如下表所示。下列说法不正确的是
| 0 min | 10 min | 20 min | 30 min | 40 min | 50 min | 60 min | |
① | 10°C | 1.1 | 0.90 | 0.80 | 0.73 | 0.68 | 0.65 | 0.65 |
② | 10°C | a | 0.70 | 0.65 | 0.65 | 0.65 | 0.65 | 0.65 |
③ | 25°C | 1.0 | 0.70 | 0.50 | 0.35 | 0.25 | 0.20 | 0.20 |
④ | 30°C | 2.0 | 1.4 | 0.90 | 0.50 | 0.20 | 0.13 | 0.13 |
A.在0~10 min内,实验③④中X的转化率相同
B.实验②中改变的条件可能是加入催化剂
C.在10~20 min内,实验①中X的平均分解速率为0.01 mol L-1min-1
D.对比实验①和④,能说明X的反应速率随温度升高而增大