题目内容
【题目】将11.2 g铁粉投入到盛有100 mL 、3 mol·L-1稀硫酸的烧杯中,4 min时铁粉刚好溶解(溶解前后溶液体积变化忽略不计),下列表示这个反应的速率正确的是
A.v(Fe)=0.5 mol/(L·min)B.v(H2SO4)=1.5 mol/(L·min)
C.v(H2SO4)=0.5 mol/(L·min)D.v(FeSO4)=1 mol/(L·min)
【答案】C
【解析】
铁粉的物质的量为![]() ,则参加反应的硫酸的物质的量也是0.1mol,故参加反应的硫酸的物质的量浓度为
,则参加反应的硫酸的物质的量也是0.1mol,故参加反应的硫酸的物质的量浓度为![]() ;根据
;根据![]() 和化学反应速率之比等化学计量数之比来解答。
和化学反应速率之比等化学计量数之比来解答。
铁粉的物质的量为![]() ,则参加反应的硫酸的物质的量也是0.1mol,故参加反应的硫酸的物质的量浓度为
,则参加反应的硫酸的物质的量也是0.1mol,故参加反应的硫酸的物质的量浓度为![]() ,
,![]() ,铁是固体,不能用于表示反应速率,
,铁是固体,不能用于表示反应速率,
故答案选:C。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
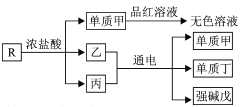
同步练习西南师范大学出版社系列答案【题目】氨气与适量氯气混合反应可生成NH4Cl(岩脑砂的主要成分)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。
A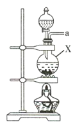 B
B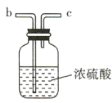
C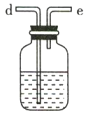 D
D
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为 ________________ 。
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→ ________________ → ________________ → ________________ → ________________ 。
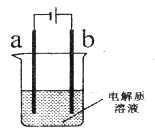
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从__________ 通入,反应的化学方程式为 ___________;可能观察到的现象是________________。
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
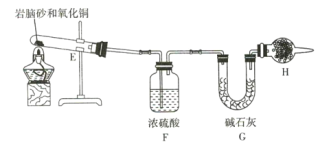
①为顺利完成有关物理量的测定,请完善下列表格。
测量时间点 | 反应前 | 反应后 |
测量内容 | ________________ | 当观察到 ________________ 现象时停止加热,冷却,称量H装置的总质量 |
②如果不用H装置,测出NH4Cl的含量将 _____ (填“偏高”“偏低”或“无影响”)。
【题目】N2O5在一定温度下可发生反应:2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是( )
A.500s内NO2的生成速率为2.96×10-3mol/(L·s)
B.T1温度下该反应平衡时N2O5的转化率为29.6%
C.平衡后,其他条件不变,将容器体积变为原来的![]() ,则c(N2O5)<5.00mol/L
,则c(N2O5)<5.00mol/L
D.T1、T2温度下的平衡常数分别为K1、K2,若T1>T2,则K1>K2