题目内容
【题目】祖母绿被称为绿宝石之王,是四大名贵宝石之一,其主要成分为Be3Al2Si6O18,因含有微量的Cr、Ni、Fe元素而呈现各种颜色。回答下列问题:
(1)祖母绿宝石属于晶体,鉴别晶体最可靠的科学方法是_____________。
(2)基态Cr原子的价层电子排布式为_________;基态Si原子电子占据最高能级的电子云轮廓图为_________。
(3)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220℃。Cr(CO)6的晶体类型是_______,1 mol Cr(CO)6中含σ键的数目为_________;
(4)BeCl2分子的空间构型是_________,写出该分子的一种等电子体的分子式_________。它的二聚体Be2Cl4结构如图所示Cl-Be![]() Be-Cl,,其中Be原子的杂化方式是_________。
Be-Cl,,其中Be原子的杂化方式是_________。
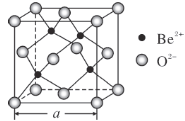
(5)BeO的立方晶胞如图所示,在该晶胞中与一个O2-距离最近且相等的O2-有________个。若该晶体的密度为d g·cm-3,设阿伏加德罗常数的值为NA,则晶胞边长a=________nm。(列出计算表达式)
(6)多数配离子显示颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量(用△表示),它与中心离子的结构、电荷、配体有关。试判断分裂能△[Fe(H2O)6]3+________ △[Fe(H2O)6]2+(填“>”、“=”或“<”),理由是___________。
【答案】X-射线衍射法 3d54s1 哑铃形或纺锤形 分子晶体 12NA 直线形 CO2 sp2 12 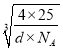 ×107 > Fe3+的3d轨道达半充满稳定状态,而Fe2+的3d轨道未达半充满稳定状态,且Fe3+所带的电荷数比Fe2+所带的电荷数多
×107 > Fe3+的3d轨道达半充满稳定状态,而Fe2+的3d轨道未达半充满稳定状态,且Fe3+所带的电荷数比Fe2+所带的电荷数多
【解析】
(1)鉴别晶体、非晶体最可靠的科学方法是X-射线衍射实验;
(2)基态Cr原子的核电荷数是24,核外电子排布式为[Ar]3d54s1;基态Si原子核外电子排布式[Ne]3s23p2,电子占据最高能级是3p能级;
(3)六羰基铬[Cr(CO)6]的沸点比较低,故该晶体为分子晶体;六羰基铬[Cr(CO)6] 中心原子Cr与配体CO之间形成配位键,配位键也是σ键,配体CO中也含有σ键;
(4)利用价层电子对数判断分子的杂化形式和分子的空间构型;
(5)根据晶胞图,8个O2-位于晶胞的顶点,6个O2-位于晶胞的面心;
(6)分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量,然后从Fe3+、Fe2+的核外电子排布去分析。
(1)鉴别晶体、非晶体最可靠的科学方法是X-射线衍射法;
(2)基态Cr原子的核电荷数是24,核外电子排布式为[Ar]3d54s1,价层电子排布式为3d54s1;基态Si原子电子占据最高能级是3p能级,电子云轮廓图为哑铃形或纺锤形;
(3)六羰基铬[Cr(CO)6]的沸点为220℃,沸点比较低,故该晶体为分子晶体;CO的结构式为![]() ,碳氧三键中1个σ键和2个π键,中心原子Cr与配体CO之间形成配位键,配位键也是σ键,故1 mol Cr(CO)6中含σ键的数目为12NA;
,碳氧三键中1个σ键和2个π键,中心原子Cr与配体CO之间形成配位键,配位键也是σ键,故1 mol Cr(CO)6中含σ键的数目为12NA;
(4)BeCl2分子的价层电子对数是2,中心原子Be采用sp杂化,故BeCl2分子的空间构型是直线形;1个BeCl2分子中含有3个原子,并且价电子数为16,CO2分子是BeCl2分子的一种等电子体;二聚体Be2Cl4结构中Be原子含有空轨道,Cl含有孤电子对,形成配位键,故二聚体Be2Cl4中Be原子的杂化方式是sp2杂化;
(5)根据晶胞图,8个O2-位于晶胞的顶点,6个O2-位于晶胞的面心,故在该晶胞中与一个O2-距离最近且相等的O2-有12个;根据晶胞图,8个O2-位于晶胞的顶点,6个O2-位于晶胞的面心,4个Be2-在体心,1个晶胞中含有Be2+的个数为4,1个晶胞中含有O2-的个数为8×(1/8)+6×(1/2)=4,(a×10-7)3 ×d×NA=4×(9+16),a=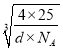 ×107;
×107;
(6)Fe3+的核外电子排布式为[Ar]3d5,3d轨道达半充满稳定状态,而Fe2+的核外电子排布式为[Ar]3d6,3d轨道未达半充满稳定状态,且Fe3+所带的电荷数比Fe2+所带的电荷数多,故分裂能△[Fe(H2O)6]3+>△[Fe(H2O)6]2+

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案【题目】氨气与适量氯气混合反应可生成NH4Cl(岩脑砂的主要成分)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。
A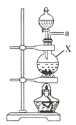 B
B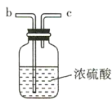
C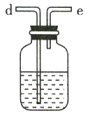 D
D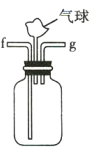
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为 ________________ 。
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→ ________________ → ________________ → ________________ → ________________ 。
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从__________ 通入,反应的化学方程式为 ___________;可能观察到的现象是________________。
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO![]() 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
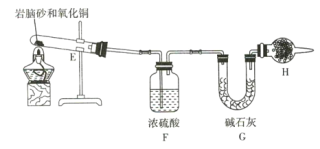
①为顺利完成有关物理量的测定,请完善下列表格。
测量时间点 | 反应前 | 反应后 |
测量内容 | ________________ | 当观察到 ________________ 现象时停止加热,冷却,称量H装置的总质量 |
②如果不用H装置,测出NH4Cl的含量将 _____ (填“偏高”“偏低”或“无影响”)。