��Ŀ����
����Ŀ����1��ICl��ICl3�Ļ�ѧ������±�����ƣ�����Ϊ±�ػ�������Ȼ��⣨ICl3������ClΪ-1�ۣ����Զ������I2Cl6��ʽ���ڣ����絼�Dzⶨ֪�����ܷ������ֵ��룬���ɵ��������ӵ�Ħ�������ֱ�Ϊ198 g/mol��269 g/mol��������뷽��ʽΪ ________________ ��
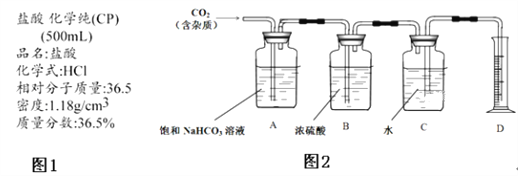
��2����ʢ��һ�������廯������Һ�����Ȼ�̼��Һ���Թ��г���ͨ����������Ӧ��Ϻ������á��ֲ㣬�����л���ʺ���ɫ��������������BrCl������ClΪ-1�ۣ������ܷ������·�Ӧ��
��2Br��+Cl2=2Cl��+Br2 ��Br2+Cl2=2BrCl ��2Fe2��+Cl2=2Fe3��+2Cl��
��ͨ�������������Ⱥ�Ӧ��˳��Ϊ ____________������ţ���
���𰸡�I2Cl6![]() ICl2��+ICl4�� �ۢ٢�
ICl2��+ICl4�� �ۢ٢�
��������
��1�����ɵ��������ӵ�Ħ�������ֱ�Ϊ198g/mol��269g/mol���ֱ�ΪICl2+��ICl4-���ܷ������ֵ��룬˵��Ϊ������ʣ�
��2�����ݻ�ԭ��ǿ���жϷ�Ӧ��˳��
��1�����Ȼ���(ICl3������ClΪ1��)���Զ������I2Cl6��ʽ���ڣ����絼�Dzⶨ֪�����ܷ������ֵ��룬���ɵ��������ӵ�Ħ�������ֱ�Ϊ198g/mol��269g/mol���ֱ�ΪICl2+��ICl4��������뷽��ʽΪI2Cl6ICl2++ICl4���ʴ�Ϊ��I2Cl6ICl2++ICl4��
��2���������ӻ�ԭ����ǿ��ͨ��������Ӧ�ȷ�����Ӧ������ͨ�����������������ӣ������巴Ӧ����BrCl����˳��Ϊ�ۢ٢ڣ��ʴ�Ϊ���ۢ٢ڡ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ�����ǵؿ��к�����21�ḻԪ�أ�������������Ԫ�أ����������Ͱ�֢��������Ѫ�ܵȾ���DZ�ڵ�ҩ��ѧ���á���ҵ���ú����۷�![]() Ϊ����ijʯúΪԭ��(����
Ϊ����ijʯúΪԭ��(����![]() ��CaO������)���ƻ��������Ʊ�
��CaO������)���ƻ��������Ʊ�![]() �����������£�
�����������£�
![]()
��֪��+5�۷�����Һ�е���Ҫ������ʽ����ҺpH�Ĺ�ϵ���±���
pH | 4~6 | 6~8 | 8~10 | 10~12 |
��Ҫ���� |
|
|
|
|
(1)���գ���ʯú�м���ʯ�ұ��գ���![]() ת��Ϊ
ת��Ϊ![]() �Ļ�ѧ����ʽ��________________��
�Ļ�ѧ����ʽ��________________��
(2)�����![]() ������ˮ�����������ᡣ����ɰ���ʱ��Һ��
������ˮ�����������ᡣ����ɰ���ʱ��Һ��![]() ��
��![]() ������������ӷ���ʽ��________________��
������������ӷ���ʽ��________________��
(3)ת����������Һ�еķ�ת��Ϊ![]() ���壬���������£�
���壬���������£�
![]()
�ٽ���Һ�м���ʯ�����������____________________________________��
����![]() ��Һ�м���
��Һ�м���![]() ��Һ��������Һ��
��Һ��������Һ��![]() ����
����![]() ʱ��
ʱ��![]() �IJ������Խ��ͣ�ԭ����_______________________________________��
�IJ������Խ��ͣ�ԭ����_______________________________________��
(4)ʵ������![]() Ϊԭ�ϻ����Ժϳ������Ʊ�
Ϊԭ�ϻ����Ժϳ������Ʊ�![]() ������(IV)��ʽ̼��茶��壬�������£�
������(IV)��ʽ̼��茶��壬�������£�
![]()
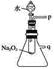
�ٲ�����������ͼװ��(����������)�н��С���֪��![]() �ܱ�
�ܱ�![]() ������
������
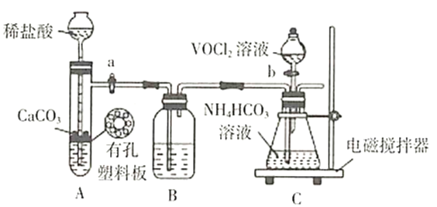
ҩƷ��װ��ɺ��ʵ�������________(��������a����������b���IJ���˳��)��װ��B�е��Լ���________��
�ڲⶨ����(IV)��ʽ̼��茶���ֲ�Ʒ�з��ĺ�����
����4.246g��Ʒ����ƿ�У���20mL����ˮ��30mL�������ܽ��![]() ��
��![]() ��Һ���Թ�������ַ�Ӧ�������1%
��Һ���Թ�������ַ�Ӧ�������1%![]() ��Һ���Թ������������س�ȥ������
��Һ���Թ������������س�ȥ������![]() �������
�������![]() ��
��![]() ����Һ�ζ����յ㣬�������Ϊ30.00mL(�ζ���Ӧ��
����Һ�ζ����յ㣬�������Ϊ30.00mL(�ζ���Ӧ��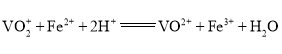 )��
)��
![]() ��Һ��������________________���ֲ�Ʒ�з�����������Ϊ________________(��ȷ��С�������λ)��
��Һ��������________________���ֲ�Ʒ�з�����������Ϊ________________(��ȷ��С�������λ)��
����Ŀ��ijС���о�NH4Cl��CuO�ķ�Ӧ����������ʵ��(����װ����)��
ʵ�� | �� | �� |
װ�� |
|
|
���� | �����Թܣ��������̣��Թܿ��а�ɫ���壻�Թ�����ˮ���ɣ��������ȣ���ɫ������������ղ��ֱ�Ϊ��ɫ | ��ϸ�����ܿڼ��������ȣ�Ѹ�ٴ�ֱ���� NH4Cl�����У�һ��ʱ���ȡ�������ܣ��ܿڴ�������ɫ���� |
����⣬ʵ����еĻ�ɫ���庬��CuCl��CuCl2��ʵ����е�����ɫ����ΪCu��
(1)ʵ������Թܿڵİ�ɫ������______��
(2)ʵ����к�ɫ������������ղ��ֹ����Ϊ��ɫ�Ĺ����У����������±仯��
![]()
��(NH4)2CuCl4�������ȷֽ�Ļ�ѧ����ʽ��______��
�ڶ�������X���������¼��裺
����X��NH4Cl��
��Ӧ����ʽΪ��________________________________(��������)
����X��______��������______��
(3)ʵ����ʵ��������ͬ�����ܵ�ԭ����______(�г�2��)��
(4)NH4Cl��Һ��CuO��Ӧ��
ʵ��� ��CuO��ĩ�м���0.1 mol��L1 NH4Cl��Һ������һ��ʱ����岿���ܽ⣬��������ɫ�仯����Һ��Ϊ��ɫ��
���ϣ������������ˮ��Һ�е���ɫ��Cu2+��ɫ��Cu(NH3)2+��Cu(NH3)42+����ɫ
����Cu(NH3)2+![]() Cu2++NH3 Cu(NH3)42+
Cu2++NH3 Cu(NH3)42+![]() Cu2++4NH3
Cu2++4NH3
�����ʵ��֤��ʵ���õ�����ɫ��Һ�д���Cu(NH3)2+��Cu(NH3)42+��
ʵ�鷽����______��
��ʵ�����δ�۲쵽NH4Cl��Һ��CuO����������ԭ��Ӧ�IJ�����ܵ�ԭ����______(�г�1�㼴��)��