题目内容
【题目】某小组研究NH4Cl与CuO的反应,进行如下实验(部分装置略):
实验 | Ⅰ | Ⅱ |
装置 |
|
|
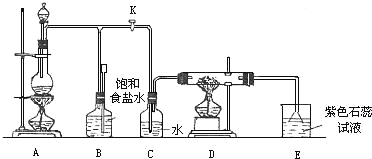
现象 | 加热试管,产生白烟,试管口有白色固体;试管中有水生成,继续加热,黑色固体变蓝,最终部分变为黄色 | 将细玻璃管口加热至红热,迅速垂直插入 NH4Cl晶体中,一段时间后,取出玻璃管,管口处有亮红色固体 |
经检测,实验Ⅰ中的黄色固体含有CuCl和CuCl2,实验Ⅱ中的亮红色固体为Cu。
(1)实验Ⅰ中试管口的白色固体是______。
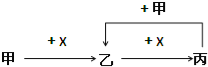
(2)实验Ⅰ中黑色固体变蓝,最终部分固体变为黄色的过程中,发生了如下变化:
![]()
①(NH4)2CuCl4固体受热分解的化学方程式是______。
②对于物质X,做出如下假设:
ⅰ.X是NH4Cl。
反应方程式为:________________________________(补充完整)
ⅱ.X是______,理由是______。
(3)实验Ⅰ和实验Ⅱ的现象不同,可能的原因是______(列出2点)。
(4)NH4Cl溶液与CuO反应。
实验Ⅲ 向CuO粉末中加入0.1 mol·L1 NH4Cl溶液,浸泡一段时间后,固体部分溶解,表面无颜色变化,溶液变为蓝色。
资料:ⅰ.相关微粒在水溶液中的颜色:Cu2+蓝色,Cu(NH3)2+和Cu(NH3)42+深蓝色
ⅱ.Cu(NH3)2+![]() Cu2++NH3 Cu(NH3)42+
Cu2++NH3 Cu(NH3)42+![]() Cu2++4NH3
Cu2++4NH3
①设计实验证明实验Ⅲ得到的蓝色溶液中存在Cu(NH3)2+或Cu(NH3)42+。
实验方案是______。
②实验Ⅲ中未观察到NH4Cl溶液与CuO发生氧化还原反应的产物,可能的原因是______(列出1点即可)。
【答案】NH4Cl (NH4)2CuCl4 ![]() CuCl2+2NH3↑+2HCl↑ 6CuCl2+2NH4Cl= 6CuCl+N2↑+ 8HCl↑ NH3 NH3有还原性 反应物的接触方式不同;反应温度不同等 取两份少量等体积的实验Ⅲ中的溶液于试管中,分别加入等量的水和稀硫酸,加入稀硫酸的溶液颜色变得更浅;取少量实验Ⅲ中的溶液于试管中,加热,溶液颜色变浅等 由于温度低等原因,NH4Cl溶液与CuO的氧化还原反应无法发生;NH4Cl溶液与CuO的氧化还原反应的化学反应速率慢、反应的限度小等
CuCl2+2NH3↑+2HCl↑ 6CuCl2+2NH4Cl= 6CuCl+N2↑+ 8HCl↑ NH3 NH3有还原性 反应物的接触方式不同;反应温度不同等 取两份少量等体积的实验Ⅲ中的溶液于试管中,分别加入等量的水和稀硫酸,加入稀硫酸的溶液颜色变得更浅;取少量实验Ⅲ中的溶液于试管中,加热,溶液颜色变浅等 由于温度低等原因,NH4Cl溶液与CuO的氧化还原反应无法发生;NH4Cl溶液与CuO的氧化还原反应的化学反应速率慢、反应的限度小等
【解析】
(1)根据氯化铵受热分解为氨气和氯化氢,氨气和氯化氢遇冷反应生成NH4Cl的原理回答;
(2) 根据(NH4)2CuCl4属于复盐,相当于2NH4Cl和CuCl2,进行分析;根据NH4Cl受热分解生成NH3和HCl,NH3又具有还原性进行分析;
(3)根据影响化学平衡移动的因素进行分析;
(1)由实验Ⅰ可知:首先是氯化铵分解为氨气和氯化氢,然后是氨气还原氧化铜,所以在中试管口的白色固体是生成的氨气和氯化氢反应生成NH4Cl,故答案:NH4Cl;
(2)①(NH4)2CuCl4属于复盐,相当于2NH4Cl和CuCl2,根据![]() 可知,固体受热分解会放出氨气、CuCl2和HCl气体,所以该反应的化学方程式是(NH4)2CuCl4
可知,固体受热分解会放出氨气、CuCl2和HCl气体,所以该反应的化学方程式是(NH4)2CuCl4 ![]() CuCl2+2NH3↑+2HCl↑,故答案:(NH4)2CuCl4
CuCl2+2NH3↑+2HCl↑,故答案:(NH4)2CuCl4 ![]() CuCl2+2NH3↑+2HCl↑;
CuCl2+2NH3↑+2HCl↑;
②ⅰ若X是NH4Cl,NH4Cl受热分解生成NH3和HCl,NH3又具有还原性,能还原CuCl2生成CuCl和N2,所以该反应方程式为:6CuCl2+2NH4Cl= 6CuCl+N2↑+ 8HCl↑,故答案为6CuCl2+2NH4Cl= 6CuCl+N2↑+ 8HCl↑;
ⅱ若X是NH3,NH3有还原性, 能还原CuCl2生成CuCl和N2,故答案:NH3;NH3有还原性;
(3)实验Ⅰ和实验Ⅱ的反应物的接触方式不同;反应温度不同,所以反应的现象不同,故答案:反应物的接触方式不同;反应温度不同等;
(4)①由Cu(NH3)2+![]() Cu2++NH3 ,且Cu2+蓝色,Cu(NH3)2+和Cu(NH3)42+深蓝色可知,加入稀硫酸,减小了氨气的量,平衡右移,铜离子的量增大,颜色变浅;或加水稀释,平衡右移,溶液的颜色的变浅;由于Cu(NH3)2+
Cu2++NH3 ,且Cu2+蓝色,Cu(NH3)2+和Cu(NH3)42+深蓝色可知,加入稀硫酸,减小了氨气的量,平衡右移,铜离子的量增大,颜色变浅;或加水稀释,平衡右移,溶液的颜色的变浅;由于Cu(NH3)2+![]() Cu2++NH3为吸热反应,所以加热平衡右移,溶液的颜色的变浅;
Cu2++NH3为吸热反应,所以加热平衡右移,溶液的颜色的变浅;
故答案为:取两份少量等体积的实验Ⅲ中的溶液于试管中,分别加入等量的水和稀硫酸,加入稀硫酸的溶液颜色变得更浅;取少量实验Ⅲ中的溶液于试管中,加热,溶液颜色变浅等;
②实验Ⅲ中未观察到NH4Cl溶液与CuO发生氧化还原反应的产物,可能由于温度低,NH4Cl溶液与CuO的氧化还原反应无法发生;或者是NH4Cl溶液与CuO的氧化还原反应的化学反应速率慢、反应的限度小等;
故答案是:由于温度低等原因,NH4Cl溶液与CuO的氧化还原反应无法发生;NH4Cl溶液与CuO的氧化还原反应的化学反应速率慢、反应的限度小等。