��Ŀ����
����Ŀ����ͼ��ij��ѧ��ȤС����Ƶ��Ҵ�������ʵ��װ��(ͼ�м�������������̨���Թܼо�δ����)��ͼ��A��Ϊ��ˮ�Ҵ�(�е�Ϊ78��)��B��Ϊ�Ƴ�����״��ϸͭ˿����˿��C��Ϊ��ˮCuSO4��ĩ��D��Ϊ��ʯ�ң�F��Ϊ���Ƶļ���Cu(OH)2����Һ��
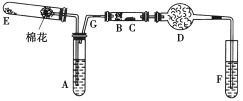
(1)������װ���У�ʵ����Ҫ���ȵ����������ȵ��Ⱥ�˳������Ϊ_______(�����)��E����һ�ִ�����䷢���Ļ�ѧ��Ӧ����ʽΪ__________��
(2)ΪʹA���Ҵ�ƽ�ȵ��������Ҵ����������õķ�����____________��D��ʹ�ü�ʯ�ҵ�������________________��
(3)��֤���Ҵ���Ӧ�������ɵIJ����������___________��
(4)ͼ��G������б��������____________��
(5)��ʵ������������E���������������䣬����C�������Ա仯����F��������(3)��ͬ��B��������Ӧ�Ļ�ѧ����ʽΪ___________��
���𰸡�E��A��B��F 2KMnO4![]() K2MnO4+MnO2+O2�� ˮԡ���� ��ֹF�е�ˮ�������뵽C�У�Ӱ��ʵ�� C�ɰ�ɫ��Ϊ��ɫ��F�г���ש��ɫ���� �û�����������˳�����뵽B�� CH3CH2OH
K2MnO4+MnO2+O2�� ˮԡ���� ��ֹF�е�ˮ�������뵽C�У�Ӱ��ʵ�� C�ɰ�ɫ��Ϊ��ɫ��F�г���ש��ɫ���� �û�����������˳�����뵽B�� CH3CH2OH![]() CH3CHO+H2��
CH3CHO+H2��
��������
��ʵ��װ�ÿ�֪���Ҵ���ͭ�������¼�������������������ԭ��Ӧ������ȩ��ˮ��ʵ����E�����Ʊ����������ɵ�����ͨ��A�У��γ��������Ҵ��Ļ�����壬��B�м��������·�Ӧ������ȩ��ˮ������C����ˮ�����ɣ������Ƶļ���Cu(OH)2����Һ�����Ƿ�������ȩ���Դ˽����⡣
(1)���������������Ҫ���ȣ��Ҵ���Ϊ��������ȣ��Ҵ��Ĵ�����Ҫ���ȣ�ȩ��Cu(OH)2����Һ�ķ�ӦҲҪ���ȣ�ʵ��ʱ��Ҫ���ȵ����������ȵ��Ⱥ�˳������ΪE��A��B��F��E����һ�ִ�����䷢����Ӧ�Ļ�ѧ����ʽΪ2KMnO4![]() K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2����
(2)ΪʹA���Ҵ�ƽ���������Ҵ������������õķ�����ˮԡ���ȣ�D��ʹ�ü�ʯ�ҵ������Ƿ�ֹF�е�ˮ�������뵽C�У�Ӱ�������ˮ�ļ��飻
(3)�Ҵ�������������ȩ��ˮ��ˮ��ʹ��ˮ����ͭ�������ڼ��������£���ȩ�����Ƶļ���Cu(OH)2����Һ��Ӧ����ש��ɫ���������C�ɰ�ɫ��Ϊ��ɫ��F�г���ש��ɫ������˵���Ҵ���������IJ�����ˮ����ȩ��
(4)G��������б�����������ڵ������������Ҵ��������Թܣ����������ܣ��û�����������˳�����뵽B�У�
(5)������E���������������䣬�����������������������Ҵ�������C�������Ա仯��˵��û������ˮ����F��������(3)��ͬ��˵���Ҵ��ֽ������ȩ����������B��������Ӧ�Ļ�ѧ����ʽ��CH3CH2OH![]() CH3CHO+H2����
CH3CHO+H2����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ����1L��0.01molNaAlO2��![]() ����Һ�л���ͨ�������̼����
����Һ�л���ͨ�������̼����![]() �����Ⱥ���������ͬ�ķ�Ӧ����0.01mol<n(CO2)��0.015molʱ�����ķ�Ӧ��:2NaAlO2+CO2+3H2O=2Al(OH)3��+Na2CO3�����ж�Ӧ��ϵ��ȷ���ǣ� ��
�����Ⱥ���������ͬ�ķ�Ӧ����0.01mol<n(CO2)��0.015molʱ�����ķ�Ӧ��:2NaAlO2+CO2+3H2O=2Al(OH)3��+Na2CO3�����ж�Ӧ��ϵ��ȷ���ǣ� ��
ѡ�� |
| ��Һ�����ӵ����ʵ���Ũ�� |
A | 0 |
|
B | 0.01 |
|
C | 0.015 |
|
D | 0.03 |
|
A.AB.BC.CD.D
����Ŀ����һ���������İ�������粒������ں��ݵ��ܱ���������У��ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4��s�� ![]() 2NH3��g����CO2��g����ʵ���ò�ͬ�¶��µ�ƽ�����������±���
2NH3��g����CO2��g����ʵ���ò�ͬ�¶��µ�ƽ�����������±���
�¶�/�� | 15 | 20 | 25 | 30 | 35 |
ƽ����ѹǿ/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
ƽ��������Ũ��/ 10-3mol��L��1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
����˵����ȷ����
A. �÷�Ӧ�ڵ����¿����Է�����
B. ����ϵ�������ƽ����Է�����������ʱ��˵���÷�Ӧ�ﵽ��ƽ��״̬
C. ���������£����������ٳ���2mol NH3��1molCO2��ƽ�������ƶ���ƽ���NH3��Ũ�ȼ�С
D. 15��ʱ���÷�Ӧ��ƽ�ⳣ��ԼΪ2.05��10-9
����Ŀ�����ǻ�ѧʵ���Ҽ����������е���Ҫ���ʣ�Ӧ�ù㷺��
��1����֪25��ʱ��N2(g)��O2(g)![]() 2NO(g) ��H=+183 kJ/mol
2NO(g) ��H=+183 kJ/mol
2H2(g)��O2(g)��2H2O(l) ��H=��571.6 kJ/mol
4NH3(g)��5O2(g)��4NO(g)��6H2O(l) ��H=��1164.4 kJ/mol
��N2(g)��3H2(g)![]() 2NH3(g) ��H=______kJ/mol
2NH3(g) ��H=______kJ/mol
��2���ں��º����ܱ������н��кϳɰ���Ӧ����ʼͶ��ʱ������Ũ�����±���
N2 | H2 | NH3 | |
Ͷ�Ϣ� | 1.0 mol/L | 3.0 mol /L | 0 |
Ͷ�Ϣ� | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
�ٰ�Ͷ�Ϣ���з�Ӧ����ôﵽ��ѧƽ��״̬ʱH2��ת����Ϊ40%������¶��ºϳɰ���Ӧ��ƽ�ⳣ������ʽΪ_______��
�ڰ�Ͷ�Ϣ���з�Ӧ����ʼʱ��Ӧ���еķ���Ϊ________�������������
���������¶ȣ���ϳɰ���Ӧ�Ļ�ѧƽ�ⳣ��________����������С�����䡱����
��L��L1��L2����X�ɷֱ����ѹǿ���¶ȡ���ͼ��ʾLһ��ʱ���ϳɰ���Ӧ��H2(g)��ƽ��ת������X�ı仯��ϵ��

�� X��������������______��
�� �ж�L1��L2�Ĵ�С��ϵ������������______��
��3���绯ѧ���������������ڼ�����NH3�ĺ������乤��ԭ��ʾ��ͼ���£�
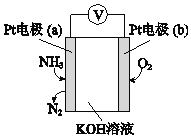
�ٵ缫b�Ϸ�������______��Ӧ�����������ԭ������
��д���缫a�ĵ缫��Ӧʽ_________��