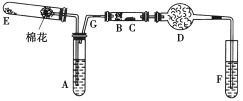
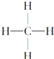��Ŀ����
����Ŀ����һ���������İ�������粒������ں��ݵ��ܱ���������У��ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4��s�� ![]() 2NH3��g����CO2��g����ʵ���ò�ͬ�¶��µ�ƽ�����������±���
2NH3��g����CO2��g����ʵ���ò�ͬ�¶��µ�ƽ�����������±���
�¶�/�� | 15 | 20 | 25 | 30 | 35 |
ƽ����ѹǿ/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
ƽ��������Ũ��/ 10-3mol��L��1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
����˵����ȷ����
A. �÷�Ӧ�ڵ����¿����Է�����
B. ����ϵ�������ƽ����Է�����������ʱ��˵���÷�Ӧ�ﵽ��ƽ��״̬
C. ���������£����������ٳ���2mol NH3��1molCO2��ƽ�������ƶ���ƽ���NH3��Ũ�ȼ�С
D. 15��ʱ���÷�Ӧ��ƽ�ⳣ��ԼΪ2.05��10-9
���𰸡�D
��������
A���ɱ��������ݿ�֪���¶�Խ�ߣ�ƽ��������Ũ�������������¶ȣ�ƽ�������ƶ�����H>0���ɻ�ѧ��������֪��S>0����H-T��S<0�ķ�Ӧ���Է����У���÷�Ӧ�ڸ����¿��Է����У�ѡ��A������
B���������а�����CO2ʼ�հ�2:1���ɣ���������ƽ����Է�������ʼ�ղ��䣬����ϵ�������ƽ����Է�����������ʱ������˵���÷�Ӧ�ﵽ��ƽ��״̬��ѡ��B������
C�����º��������£���ԭƽ����ϵ���ٳ���2molNH3��1molCO2��ƽ�������ƶ�����ԭƽ��ʱ�����������ʵ�������ͬ����ƽ���NH3Ũ�Ȳ��䣬ѡ��C����
D��15��ʱ��ƽ��������Ũ��Ϊ2.4��10-3mol/L����Ϸ�Ӧ��֪c(NH3)=1.6��10-3 mol/L�� c(CO2)=0.8��10-3mol/L��K= (1.6��10-3mol/L)2��0.8��10-3mol/L=2.05��10-9 (mol/L)3��ѡ��D��ȷ��
��ѡD��

 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д�����Ŀ����������ʵ��������������ó��Ľ�����ȷ����
ѡ�� | ʵ����������� | ���� |
A | ����Һ�еμ�Na2CO3��Һ����Һ���� | ���ӵ�����ǿ��H2CO3������ |
B | ���ˮ�м�������CCl4�����ã��ϲ�ӽ���ɫ���²����Ϻ�ɫ | I2��CCl4�е��ܽ�ȴ�����ˮ�е��ܽ�� |
C | ��CuSO4��Һ�м������ۣ��к�ɫ�������� | Fe2+��������ǿ��Cu2+�������� |
D | ��NaCl��NaI�Ļ��ϡ��Һ�е�������ϡAgNO3��Һ���л�ɫ�������� | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D
����Ŀ���ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϡ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
CH4(g)+H2O(g)![]() CO(g)+3H2(g) ��H1=+206.1kJ/mol ��
CO(g)+3H2(g) ��H1=+206.1kJ/mol ��
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ��H2=+247.3kJ/mol ��
2CO(g)+2H2(g) ��H2=+247.3kJ/mol ��
��ش��������⣺
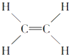
(1)��һ�ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5min�ڣ�v(H2)=____��10minʱ���ı���������������_____��
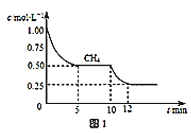
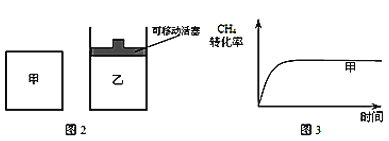
(2)��ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������CH4��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������CH4��ת������ʱ��仯��ͼ��_____��
(3)800��ʱ����ӦCO(g)+H2O(g)![]() CO2(g)+H2(g)�Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±�����ʱ��Ӧ�������淴Ӧ���ʵĹ�ϵʽ��____������ţ���
CO2(g)+H2(g)�Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±�����ʱ��Ӧ�������淴Ӧ���ʵĹ�ϵʽ��____������ţ���
a.v(��)��v(��)
b.v(��)��v(��)
c.v(��)=v(��)
d.���ж�
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
(4)�����ѣ�CH3OCH3�����ɺϳ�����CO��H2����һ���������Ƶã�д���÷�Ӧ�Ļ�ѧ����ʽ��____��
(5)�Զ����ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫����ȼ�ϵ�ء��õ�صĸ����缫��Ӧ����ʽ�ǣ�____���ö�����ȼ�ϵ��Ϊ��Դ���ò��缫���KCl��CuSO4�Ļ����Һ������·��ͨ��0.3mol���ӵĵ���ʱ����������������2.8L������(��״��)����������Һ���Ϊ1L������������ijɷּ����ʵ���Ϊ��____��