题目内容
【题目】Al3+与CO32-不能大量共存是它们相互促进水解完全造成的么?__________
【答案】是
【解析】
Al3+水解消耗OH-,CO32-水解消耗H+,OH-与H+结合生成H2O,使离子水解促进,结合溶液的酸碱性及离子浓度变化分析。
Al3+是强酸盐电离产生,Al3+会发生水解反应,消耗水电离产生的OH-,水解方程式为:Al3++3H2O![]() Al(OH)3+3H+,水解产生H+,使溶液显酸性;
Al(OH)3+3H+,水解产生H+,使溶液显酸性;
CO32-是强碱盐电离产生,CO32-会发生水解反应,消耗水电离产生的H+,反应产生OH-、HCO3-,HCO3-进一步水解产生H2CO3、OH-,水解方程式为:CO32-+H2O![]() HCO3-+OH-,HCO3-进一步发生水解反应:HCO3-+H2O
HCO3-+OH-,HCO3-进一步发生水解反应:HCO3-+H2O![]() H2CO3+OH-,当达到水解平衡时,溶液中c(OH-)>c(H+),溶液显碱性;含有Al3+的溶液与含有的CO32-溶液混合时,水解产生的H+、OH-发生中和反应,使二者水解程度都增大,最终彻底、完全,产生Al(OH)3沉淀和H2CO3,H2CO3不稳定,分解产生CO2气体,反应方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑,可见两种离子由于盐的双水解反应而不能大量共存。
H2CO3+OH-,当达到水解平衡时,溶液中c(OH-)>c(H+),溶液显碱性;含有Al3+的溶液与含有的CO32-溶液混合时,水解产生的H+、OH-发生中和反应,使二者水解程度都增大,最终彻底、完全,产生Al(OH)3沉淀和H2CO3,H2CO3不稳定,分解产生CO2气体,反应方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑,可见两种离子由于盐的双水解反应而不能大量共存。

【题目】合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1=+206.1kJ/mol ①
CO(g)+3H2(g) ΔH1=+206.1kJ/mol ①
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH2=+247.3kJ/mol ②
2CO(g)+2H2(g) ΔH2=+247.3kJ/mol ②
请回答下列问题:
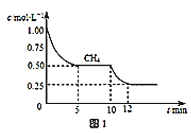
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。反应进行的前5min内,v(H2)=____;10min时,改变的外界条件可能是_____。
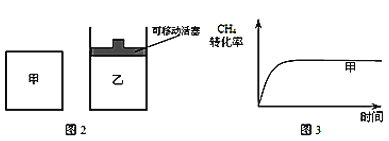
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像_____。
(3)800℃时,反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表,此时反应中正、逆反应速率的关系式是____(填序号)。
CO2(g)+H2(g)的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表,此时反应中正、逆反应速率的关系式是____(填序号)。
a.v(正)>v(逆)
b.v(正)<v(逆)
c.v(正)=v(逆)
d.无法判断
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
(4)二甲醚(CH3OCH3)可由合成气(CO和H2)在一定条件下制得,写出该反应的化学方程式:____。
(5)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池。该电池的负极电极反应方程式是:____。用二甲醚燃料电池为电源,用铂电极电解KCl和CuSO4的混合溶液,当电路中通过0.3mol电子的电量时,阴阳两极都产生2.8L的气体(标准状况),若电解后溶液体积为1L,则阳极气体的成分及物质的量为:____。