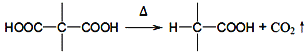题目内容
【题目】下列化学用语对事实的表述正确的是
A.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
B.向Na2SiO3溶液中通入过量的SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32-
C.由Na和C1形成离子键的过程:![]()
D.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32-
【答案】C
【解析】
A.硬脂酸为C17H35COOH,含有羧基,与C2H518OH发生酯化反应,乙醇脱去H原子,硬脂酸脱去羟基,反应的化学方程式为C17H35COOH+C2H518OH![]() C17H35CO18OC2H5+H2O,故A错误;
C17H35CO18OC2H5+H2O,故A错误;
B.向Na2SiO3溶液中通入过量SO2的离子反应为SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3-,故B错误;
C.氯化钠为离子化合物,含有离子键,反应中Na失去电子,Cl得到电子,则Na和Cl形成离子键的过程:![]() →
→![]() ,故C正确;
,故C正确;
D.弱酸的电离平衡常数越大,酸的酸性越强,强酸能和弱酸盐反应生成弱酸,所以向NaClO溶液中通入少量CO2:ClO-+CO2+H2O═HClO+HCO3-,故D错误;
故答案为C。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目