题目内容
4.能形成A2B型离子化合物的两种元素的原子序数是( )| A. | 20和8 | B. | 1和6 | C. | 11和16 | D. | 12和17 |
分析 活泼金属和活泼非金属之间易形成离子键,非金属元素之间易形成共价键(铵盐除外),含有离子键的化合物是离子化合物,A2B型离子化合物中A显+1价,B显-2价.
解答 解:A、20号元素是Ca元素,8号元素是O元素,这形成化合物CaO,不是A2B型,故A错误;
B、6号元素是C元素,1号元素是H元素,所以这两种元素不能形成离子化合物,故B错误;
C、11号元素是Na元素,16号元素是S元素,硫化钠是离子化合物,所以形成的离子化合物是A2B型离子化合物,故C正确;
D、12号元素是Mg元素,镁是活泼金属;17号元素是Cl元素,Cl是活泼非金属,所以形成的氟化镁是离子化合物;氯化镁中镁显+2价,Cl显-1价,所以氯化镁是AB2型离子化合物,故D错误.
故选C.
点评 本题考查了离子键、共价键的判断,难度不大,注意先根据原子序数判断元素,再根据化合价判断是否符合题意.

练习册系列答案
相关题目
14.下列指定微粒的个数比为2:1的是( )
| A. | 2H原子中的中子和质子 | |
| B. | Be2+离子中的质子和电子 | |
| C. | NaHCO3晶体中的阳离子和阴离子 | |
| D. | BaO2(过氧化钡)固体中的阴离子和阳离子 |
15.反应C(s)+H2O(g)?CO(g)+H2(g)在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加C的量 | B. | 将容器的体积缩小一半 | ||
| C. | 保持容器体积不变,充入N2 | D. | 保持容器体积不变,充入H2O(g) |
12.下列物质以任意比例混合,若总物质的量一定,则充分燃烧消耗氧气及生成水的量均相等的是( )
| A. | C2H6,C2H6O | B. | C3H6,C4H6O2 | C. | C2H2,C2H4O | D. | C3H6O,C4H8O2 |
19.关于如图图示的说法中正确的是( )
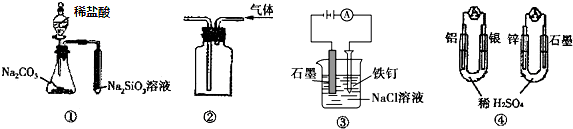

| A. | 用图①所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集CH4气体 | |
| C. | 装置③可电解食盐水制氯气 | |
| D. | 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
9.下列有关化学用语表示正确的是( )
| A. | 甲醛的电子式: | B. | 对甲基苯酚的结构简式: | ||
| C. | 乙醇分子的比例模型: | D. | 3,3-二甲基-1-戊烯的键线式: |
14.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 在1 mol NaHSO4晶体中,含阳离子数为2NA | |
| B. | 1 mol C4H10分子中共价键总数为13NA | |
| C. | 0.5 mol•L-1 Ba(NO3)2溶液中,NO${\;}_{3}^{-}$的数目为NA | |
| D. | 任何条件下,20 L N2含有的分子数都不可能为NA |
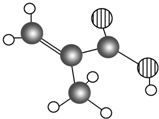 某化工厂产品只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键,如单键、双键等).
某化工厂产品只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键,如单键、双键等). .
.