题目内容
12.下列物质以任意比例混合,若总物质的量一定,则充分燃烧消耗氧气及生成水的量均相等的是( )| A. | C2H6,C2H6O | B. | C3H6,C4H6O2 | C. | C2H2,C2H4O | D. | C3H6O,C4H8O2 |
分析 只要混合物的总物质的量一定,完全燃烧消耗O2的量保持不变,则1mol各组分消耗氧气的量相等;总物质的量一定生成水的量不变,则有机物分子中含有的H原子数目一定相等,据此进行解答.
解答 解:混合物的总物质的量一定,完全燃烧生成水的量和消耗O2的量均不变,则1mol各组分消耗氧气的量相等,分子中含有的氢原子数目相等,
A.C2H6、C2H6O分子中C、H原子数相同,后者含有氧原子,则等物质的量的二者耗氧量不同,故A错误;
B.C3H6、C4H6O2分子中,C4H6O2改写为C3H6.CO2,C3H6.CO2、C3H6分子中含有H原子数相等,且1mol时消耗的氧气都是4.5mol,所以只要混合物的总物质的量一定,则完全燃烧时生成水的量和消耗O2的量均相等,故B正确;
C.C2H2、C2H4O分子中含有H原子数不相等,物质的量组成不同时,燃烧生成水的物质的量不相等,不符合题意,故C错误;
D.C3H6O,C4H8O2分子中含有H原子数不相等,物质的量组成不同时,燃烧生成水的物质的量不相等,不符合题意,故D错误;
故选B.
点评 本题考查了有关混合物反应的计算,侧重考查有机物分子式的确定,题目难度中等,明确“总物质的量一定,则充分燃烧消耗氧气及生成水的量均相等”的含义为解答关键,B注意掌握拆分法的应用,可以简化计算过程.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
2. 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )| A. | O2在电极b上发生还原反应 | |
| B. | 溶液中OH-向电极a移动 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | 负极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O |
3.元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于S2-的半径,X元素为( )
| A. | Al | B. | P | C. | K | D. | Ar |
20.只用水就能鉴别的一组物质是( )
| A. | 苯、乙酸、四氯化碳 | B. | 乙醇、乙醛、乙酸 | ||
| C. | 溴苯、乙二醇、硝基苯 | D. | 乙酸乙酯、乙醇、甘油 |
7.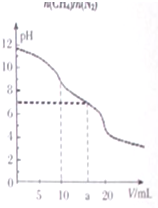 常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
 常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-) | |
| B. | 当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-) | |
| C. | 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-) |
17.下列有关原电池的说法正确的是( )
| A. | 原电池中由电能转化为化学能 | B. | 原电池中失电子的电极作负极 | ||
| C. | 原电池的负极发生还原反应 | D. | 原电池中电子由正极流向负极 |
4.能形成A2B型离子化合物的两种元素的原子序数是( )
| A. | 20和8 | B. | 1和6 | C. | 11和16 | D. | 12和17 |
2.往Na2S、Na2SO3的混合物中加入稀硫酸,反应中不可能生成的物质是( )
| A. | S | B. | SO2 | C. | H2S | D. | SO3 |
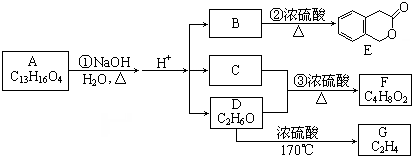
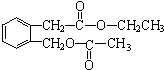 ;B的分子式是C9H10O3.
;B的分子式是C9H10O3. 、
、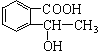 、
、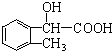 .
. .
.