题目内容
15.反应C(s)+H2O(g)?CO(g)+H2(g)在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )| A. | 增加C的量 | B. | 将容器的体积缩小一半 | ||
| C. | 保持容器体积不变,充入N2 | D. | 保持容器体积不变,充入H2O(g) |
分析 对应反应C(s)+H2O(g)?CO(g)+H2(g),有气体参加和生成,则温度、压强、浓度都能对化学反应速率产生影响,以此来解答.
解答 解:A、碳为纯固体,改变其用量,对化学反应速率无影响,故A选;
B、将容器的体积缩小一半,相当于压强增大,则反应速率加快,故B不选;
C、保持体积不变,充入氮气,反应物和生成物浓度不变,反应速率不变,故C选;
D、容器体积不变充入H2O(g)反应物浓度增大,反应速率加快,故D不选;
故选AC.
点评 影响化学速率的因素有:温度、浓度、压强、催化剂、固体表面积,需要注意的是改变纯固体或液体的量,对反应速率无影响,压强改变必须引起浓度的改变才能引起化学反应速率的改变.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.化学与生活密切相关,下列说法正确的是( )
| A. | 福尔马林可用作食品防腐剂 | |
| B. | 苯酚皂可用于环境消毒,医用酒精可用于皮肤消毒,其原因是它们都可以杀死细菌 | |
| C. | “乙醇汽油”是在汽油中加入乙醇生成的一种新化合物 | |
| D. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 |
3.元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于S2-的半径,X元素为( )
| A. | Al | B. | P | C. | K | D. | Ar |
20.只用水就能鉴别的一组物质是( )
| A. | 苯、乙酸、四氯化碳 | B. | 乙醇、乙醛、乙酸 | ||
| C. | 溴苯、乙二醇、硝基苯 | D. | 乙酸乙酯、乙醇、甘油 |
7.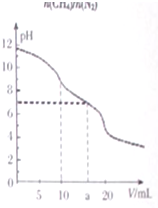 常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
 常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用VmL0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-) | |
| B. | 当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-) | |
| C. | 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-) |
4.能形成A2B型离子化合物的两种元素的原子序数是( )
| A. | 20和8 | B. | 1和6 | C. | 11和16 | D. | 12和17 |
5.下表列出了A-R9种元素在周期表中的位置
(1)这九种元素中:化学性质最不活泼的是Ar;金属性最强的是:K,最高价氧化物的水化物碱性最强的碱的电子式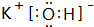 ,最高价氧化物的水化物酸性最强的酸是HClO4;氢化物稳定性最差的是CH4
,最高价氧化物的水化物酸性最强的酸是HClO4;氢化物稳定性最差的是CH4
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应的水化物反应的离子方程式是Al(OH)3+OH-=AlO2-+2 H2O
(3)A、B、C三种元素按原子半径由大到小的顺序排列为K>Na>Mg,离子半径顺序为:K+>Na+>Mg2+
(4)F的最常见氢化物的电子式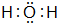 ;该氢化物在常温下跟B发生反应的化学方程式是2K+2 H2O=2KOH+H2↑,剧烈程度大于(填大于、小于、等于)A.
;该氢化物在常温下跟B发生反应的化学方程式是2K+2 H2O=2KOH+H2↑,剧烈程度大于(填大于、小于、等于)A.
(5)C元素跟G元素形成的化合物的电子式是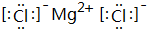 ,用电子式表示其形成过程为
,用电子式表示其形成过程为 .
.
(6)G元素和H元素,A元素和B元素核电荷数之差分别为18、8.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
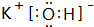 ,最高价氧化物的水化物酸性最强的酸是HClO4;氢化物稳定性最差的是CH4
,最高价氧化物的水化物酸性最强的酸是HClO4;氢化物稳定性最差的是CH4(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应的水化物反应的离子方程式是Al(OH)3+OH-=AlO2-+2 H2O
(3)A、B、C三种元素按原子半径由大到小的顺序排列为K>Na>Mg,离子半径顺序为:K+>Na+>Mg2+
(4)F的最常见氢化物的电子式
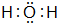 ;该氢化物在常温下跟B发生反应的化学方程式是2K+2 H2O=2KOH+H2↑,剧烈程度大于(填大于、小于、等于)A.
;该氢化物在常温下跟B发生反应的化学方程式是2K+2 H2O=2KOH+H2↑,剧烈程度大于(填大于、小于、等于)A.(5)C元素跟G元素形成的化合物的电子式是
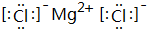 ,用电子式表示其形成过程为
,用电子式表示其形成过程为 .
.(6)G元素和H元素,A元素和B元素核电荷数之差分别为18、8.