题目内容
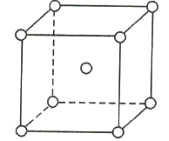
【题目】元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体的晶胞结构如图所示。

(1)该晶体的阳离子与阴离子个数比为____。
(2)该晶体中Xn+中n=____。
(3)X元素的原子序数是_____。
(4)晶体中每个N3-被____个等距离的Xn+包围。
【答案】3∶1 1 29 6
【解析】
(1)Xn+位于晶胞的棱上,其个数为12×![]() =3,N3-位于晶胞的顶角,其个数为8×
=3,N3-位于晶胞的顶角,其个数为8×![]() =1,故Xn+与N3-的个数比为3∶1;
=1,故Xn+与N3-的个数比为3∶1;
(2)由晶体的化学式X3N知X的所带电荷为1;
(3)因为X+的K、L、M三个电子层充满,故为2、8、18,所以X的原子序数是29;
(4)N3-位于晶胞顶角,故其被6个Xn+在上、下、左、右、前、后包围,故答案为6。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目