题目内容
12.下列除去杂质的方法正确的是( )| A. | 除去BaSO4中的少量BaCO3加入足量盐酸,充分反应后,过滤、洗涤、干燥 | |
| B. | 除去KCl溶液中的少量MgCl2,加入适量NaOH溶液,过滤 | |
| C. | 除去CO2气体中混有的HCl气体:通过饱和碳酸氢钠溶液,洗气 | |
| D. | 除去碘水中的碘,加入乙醇萃取后分液 |
分析 A.BaCO3与盐酸反应生成可溶性物质,而BaSO4不溶于酸和水;
B.MgCl2与NaOH反应生成沉淀和NaCl;
C.HCl与碳酸氢钠反应生成二氧化碳;
D.乙醇与水互溶.
解答 解:A.BaCO3与盐酸反应生成可溶性物质,而BaSO4不溶于酸和水,则加入足量盐酸,充分反应后,过滤、洗涤、干燥可除杂,故A正确;
B.MgCl2与NaOH反应生成沉淀和NaCl,引入新杂质NaCl,应选加入适量KOH溶液,过滤来除杂,故B错误;
C.HCl与碳酸氢钠反应生成二氧化碳,则通过饱和碳酸氢钠溶液,洗气可除杂,故C正确;
D.乙醇与水互溶,不能作萃取剂,应加入苯或四氯化碳萃取,故D错误;
故选AC.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的化学反应为解答的关键,侧重分析与应用能力的综合考查,注意除杂的原则,题目难度不大.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
3.可以用来鉴别乙烷和乙烯,还可以用来除去乙烷中乙烯的操作方法是( )
| A. | 将混合气体通过盛有浓硫酸的洗气瓶 | |
| B. | 将混合气体通过盛有水的洗气瓶 | |
| C. | 将混合气体通过盛有足量溴水的洗气瓶 | |
| D. | 将混合气体通过盛有澄清石灰水的洗气瓶 |
7.碳酸铜和碱式碳酸铜〔Cu2(OH)2CO3〕均可溶于盐酸,转化为氯化铜.在高温下这两种化合物均能分解生成氧化铜.溶解28.4g的上述混合物,消耗2mol•L-1的盐酸250mL.灼烧等量的上述混合物,得到氧化铜的质量是( )
| A. | 40 g | B. | 30 g | C. | 20 g | D. | 15 g |
17.下列描述中,不符合生产实际的是( )
| A. | 工业电解饱和食盐水,阳离子交换膜的作用是使得阴极区的OH -不能进入阳极区 | |
| B. | 电解法精炼铜用纯铜作阴极,阳极泥中可能含有金、银等贵重金属. | |
| C. | 在镀件上电镀锌,用锌作阳极 | |
| D. | 电解熔融的氧化铝制取金属铝,用铁作阳极 |
2.下列表述中正确的是( )
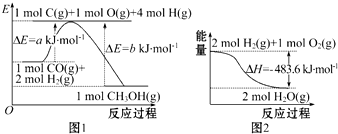

| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 | |
| C. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
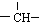 和一个-Cl,它的可能结构有四种,请写出它们的结构简式:CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.
和一个-Cl,它的可能结构有四种,请写出它们的结构简式:CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.