题目内容
如图为相互串联的甲、乙两个电解池.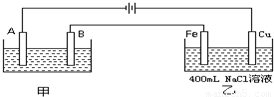
试回答:
(1)若甲池利用电解原理在铁上镀银,则A是______、______(依次填电极材料和电极名称),电极反应是______;B是______、______(依次填电极材料和电极名称),电极反应是______;应选用的电解质溶液是______.
(2)若甲池阴极增重43.2g且乙池中阴极上一直都有气体产生,则乙池中阴极上放出的气体在标准状况下的体积是______L.
【答案】分析:(1)由图可知,A与电源负极相连,则A为阴极,甲池利用电解原理在铁上镀银,则铁应作负极,银作正极,电解液中含有银离子,以此来分析;
(2)利用电子守恒可知2Ag~2e-~H2↑,以此来计算氢气的物质的量,再计算气体在标准状况下的体积.
解答:解:(1)由图可知,A与电源负极相连,则A为阴极,在铁上镀银,则铁作阴极,电极反应为Ag++e-=Ag,
银作正极,电极反应为Ag-e-=Ag+,且电解液中含有银离子,可选AgNO3作电解液,
故答案为:Fe;阴极;Ag++e-=Ag;Ag;阳极;Ag-e-=Ag+;AgNO3;
(2)甲池阴极发生Ag++e-=Ag,乙池中阴极2H++e-=H2↑,
Ag的物质的量为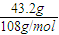 =0.4mol,
=0.4mol,
由电子守恒可知,2Ag~2e-~H2↑,氢气的物质的量为0.2mol,
在标准状况下的体积为0.2mol×22.4L/mol=4.48L,故答案为:4.48.
点评:本题考查电解原理及利用电子守恒的计算,明确阴阳极的判断及发生的电极反应是解答本题的关键,难度不大.
(2)利用电子守恒可知2Ag~2e-~H2↑,以此来计算氢气的物质的量,再计算气体在标准状况下的体积.
解答:解:(1)由图可知,A与电源负极相连,则A为阴极,在铁上镀银,则铁作阴极,电极反应为Ag++e-=Ag,
银作正极,电极反应为Ag-e-=Ag+,且电解液中含有银离子,可选AgNO3作电解液,
故答案为:Fe;阴极;Ag++e-=Ag;Ag;阳极;Ag-e-=Ag+;AgNO3;
(2)甲池阴极发生Ag++e-=Ag,乙池中阴极2H++e-=H2↑,
Ag的物质的量为
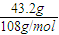 =0.4mol,
=0.4mol,由电子守恒可知,2Ag~2e-~H2↑,氢气的物质的量为0.2mol,
在标准状况下的体积为0.2mol×22.4L/mol=4.48L,故答案为:4.48.
点评:本题考查电解原理及利用电子守恒的计算,明确阴阳极的判断及发生的电极反应是解答本题的关键,难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
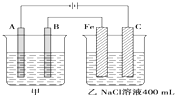 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: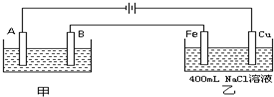
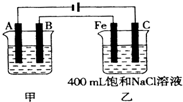 如图为相互串联的甲、乙两电解池.试回答:
如图为相互串联的甲、乙两电解池.试回答: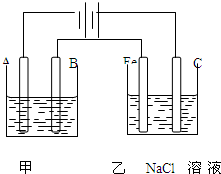 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: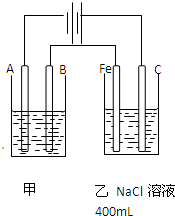 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: