题目内容
12.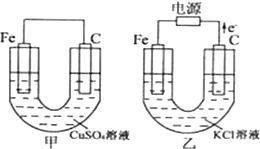 根据如图所提供的信息,在反应一段时间后:
根据如图所提供的信息,在反应一段时间后:(1)甲池中的现象为:铁棒逐渐溶解,碳棒上有红色物质析出,蓝色溶液逐渐变浅.
(2)乙池中总反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-.
(3)将湿润的淀粉KI试纸放在乙池碳棒附近,发现试纸变蓝,其原因是:(用离子方程式表示)Cl2+2I-═I2+2Cl-;但过一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2又氧化.若反应的Cl2和I2物质的量之比为5:1,且生成两种酸,该反应的化学方程式为:5Cl2+I2+6H2O═2HIO3+10HCl.
(4)若乙池的电源连接方向开始时就与上述的图示相反,则反应一段时间后,其溶液中可能出现的现象是产生白色絮状沉淀.
(5)现有200mL食盐水,用石墨电极电解.当阴极产生气体的体积为0.224L(标准状况)时停止电解,阳极的电极反应式为2C1--2e-=C12↑,电解后,溶液在常温下的pH约为13(忽略体积变化).
分析 (1-4)由图可知,甲为原电池,负极为Fe,电池反应为Fe+Cu2+═Fe2++Cu,乙为电解池,由电子流向正极可知,C为阳极,Fe为阴极,电解反应为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-,以此来解答;
(5)电解食盐水时,C1-在阳极失电子生成氯气;阴极生成氢气,根据氢气的量求出氢氧化钠的量,然后求出PH.
解答 解:(1)甲中发生Fe+Cu2+═Fe2++Cu,观察到铁棒逐渐溶解,碳棒上有红色物质析出,蓝色溶液逐渐变浅,
故答案为:铁棒逐渐溶解,碳棒上有红色物质析出,蓝色溶液逐渐变浅;
(2)乙为电解池,由电子流向正极可知,C为阳极,Fe为阴极,电解反应为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-,故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-;
(3)乙池碳棒附近氯离子放电生成氯气,氯气氧化KI生成碘单质遇淀粉变蓝,离子反应为Cl2+2I-═I2+2Cl-,过量的Cl2将生成的I2又氧化.若反应的Cl2和I2物质的量之比为5:1,且生成两种酸,Cl元素的化合价降低,生成盐酸,I元素的化合价升高,由电子守恒可知,5×2×(1-0)=1×2×(x-0),解得x=+5,生成物为碘酸,该化学反应为5Cl2+I2+6H2O═2HIO3+10HCl,
故答案为:Cl2+2I-═I2+2Cl-;5Cl2+I2+6H2O═2HIO3+10HCl;
(4)若乙池的电源连接方向开始时就与上述的图示相反,则Fe为阳极,失去电子,阴极氢离子放电生成氢气,生成的亚铁离子与氢氧根离子反应生成氢氧化亚铁,观察到产生白色絮状沉淀,故答案为:产生白色絮状沉淀;
(5)电解食盐水时,C1-在阳极失电子生成氯气,其电极反应式为:2C1--2e-=C12↑;阴极生成氢气,n(H2)=$\frac{0.224L}{22.4L/mol}$=0.01mol;已知2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,当产生的H2的体积为0.224L即0.01mol时,生成氢氧化钠的物质的量为0.02mol,所以溶液中NaOH的物质的量浓度=$\frac{0.02mol}{0.2L}$=0.1mol/L,所以氢离子的浓度为1×10-13mol/L,pH=13,故答案为:2C1--2e-=C12↑;13.
点评 本题考查原电池和电解池,装置的判断是解答的关键,注意把握原电池和电解池的工作原理,明确离子的放电顺序及发生的电极反应即可解答,题目难度中等.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案| A. | 1,2-二溴乙烷 | B. | 2,3-二甲基丁烷 | ||
| C. | 2-丁烯 | D. | 2-甲基-3-乙基丁烷 |
| A. | 反应中共转移电子3mol | |
| B. | 反应中共消耗锌97.5 g | |
| C. | 气体A中SO2和H2的体积比为4:1 | |
| D. | 稀释后的溶液中c(SO42-)=1.55 mol•L-1 |
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g);△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
| A. | CO的燃烧热为283kJ | |
| B. | 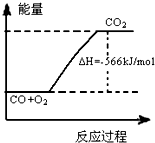 如图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | Na2O2(s)+CO(g)=Na2CO3(s);△H=-509kJ/mol | |
| D. | Na2O2(s)与CO2(g)反应放出226kJ热量时,电子转移数为2NA |
| A. | CO32-、H+、HCO3-、Ca2+ | B. | NH4+、OH-、Ba2+、NO3- | ||
| C. | I-、ClO-、NO3-、H+ | D. | SO32-、SO42-、Na+、OH- |
| A. | 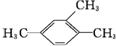 1,3,4-三甲苯 1,3,4-三甲苯 | B. | 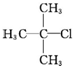 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | C. | 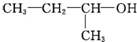 2-丁醇 2-丁醇 | D. | 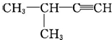 2-甲基-3-丁炔 2-甲基-3-丁炔 |