题目内容
12.设阿伏加德罗常数的值为NA,下列说法中正确的是( )| A. | 标准状况下,2.24LCHCl3含有的分子数为0.1NA | |
| B. | 0.1molCmH2n+2中含有的碳碳单键数为0.1nNA | |
| C. | 2.8g乙烯和丙烯的混合气体中所含碳原子为0.2NA | |
| D. | 1mol苯乙烯中含有的碳碳双键数为4NA |
分析 A、标况下,三氯甲烷为液态;
B、1molCmH2n+2中含有(m-1)mol碳碳单键;
C、乙烯和丙烯的最简式均为CH2;
D、苯环不是单双键交替结构.
解答 解:A、标况下,三氯甲烷为液态,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、1molCmH2n+2中含有(m-1)mol碳碳单键,故0.1molCmH2n+2中含有0.1(m-1)mol碳碳单键,故B错误;
C、乙烯和丙烯的最简式均为CH2,故2.8g混合物中含有的CH2的物质的量n=$\frac{2.8g}{14g/mol}$=0.2mol,故含有0.2mol碳原子,即0.2NA个,故C正确;
D、苯环不是单双键交替结构,故1mol苯乙烯中含1mol碳碳双键,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
17. 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )
 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )| A. | X为直流电源的负极,Y为直流电源的正极 | |
| B. | 阳极区pH增大 | |
| C. | 图中的b>a | |
| D. | 该过程中的产品还有H2SO4 |
3.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5;④1s22s22p63s23p2则下列有关比较中正确的是( )
| A. | 第一电离能:③>②>④>① | B. | 原子半径:①>②>④>③ | ||
| C. | 电负性:③>①>②>④ | D. | 最高正化合价:③>①>②>④ |
20.在正规考试化学试卷的试题前总有“可能用到的相对原子质量”一项,如H-1 C-12 Cl-35.5 N-14等.请问这些数据准确的说法应该是( )
| A. | 某种核素的相对原子质量 | |
| B. | 某种核素的质量数 | |
| C. | 某种元素所有核素质量数的平均值 | |
| D. | 某种元素的平均相对原子质量的近似值 |
17.对11→17号元素性质的描述正确的是( )
| A. | 原子半径和简单离子半径减小 | |
| B. | 氧化物对应的水化物碱性减弱,酸性增强 | |
| C. | 14号元素的高纯单质可制光电池 | |
| D. | 单质的熔点降低 |
4.下列有机物在常温下呈液态的是( )
| A. | CH3(CH2)4CH3 | B. | C18H38 | C. | C3H6 | D. | CH3Cl |
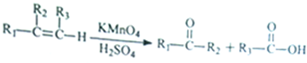 由
由 到
到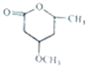 的合成路线如下所示:
的合成路线如下所示:
 ;B
;B ;C
;C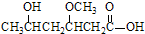 .
.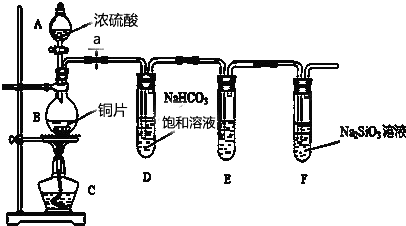


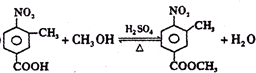 ,使用过量CH3OH的作用是提高D的产率.
,使用过量CH3OH的作用是提高D的产率.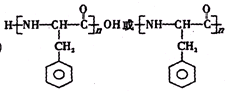 .
.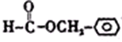 .
.