题目内容
20.在正规考试化学试卷的试题前总有“可能用到的相对原子质量”一项,如H-1 C-12 Cl-35.5 N-14等.请问这些数据准确的说法应该是( )| A. | 某种核素的相对原子质量 | |
| B. | 某种核素的质量数 | |
| C. | 某种元素所有核素质量数的平均值 | |
| D. | 某种元素的平均相对原子质量的近似值 |
分析 我们平常所说的某种元素的相对原子质量,是按各种天然同位素原子所占的一定百分比算出来的平均值.
解答 解:在正规化学试卷的开始处总有“可能用到的相对原子质量”,是元素的相对原子质量的近似值,按各种天然同位素原子所占的一定百分比算出来的平均值的近似值,
故选D.
点评 本题主要考查了元素的相对原子质量,难度不大,注意概念的区分.

练习册系列答案
相关题目
8.金属锂燃料电池是一种新型电池,比锂离子电池具有更高的能量密度.它无电时也无需充电,用作燃料电池时,可更换正极的水性电解液和卡盒以及负极的金属锂就可以连续使用,分离出的氢氧化锂可采用电解其熔融物法回收锂而循环使用.其工作示意图如右图,下列说法不正确的是( )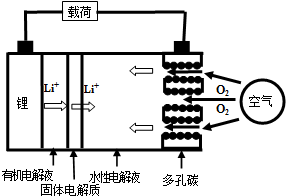

| A. | 放电时负极的电极反应式为:Li-e-=Li+ | |
| B. | 熔融的氢氧化锂用惰性电极电解再生时,金属锂在阴极得到 | |
| C. | 有机电解液可以是乙醇等无水有机物 | |
| D. | 放电时,正极的电极反应式为:2H2O+O2+4e-=4OH- |
15.下列有关化学用语的表示错误的是( )
| A. | 甲烷的比例模型: | B. | 氯离子的结构示意图: | ||
| C. | 溴原子的价层电子排布式:4s24p5 | D. | 过氧化钠的电子式: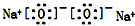 |
5.m mol乙炔跟n mol氢气在密闭容器中反应,当其达到平衡时生成p mol乙烯,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是( )
| A. | (3m+n)mol | B. | (3m+n+2p)mol | C. | (2.5m+0.5n-3p)mol | D. | (2.5m+0.5n)mol |
12.设阿伏加德罗常数的值为NA,下列说法中正确的是( )
| A. | 标准状况下,2.24LCHCl3含有的分子数为0.1NA | |
| B. | 0.1molCmH2n+2中含有的碳碳单键数为0.1nNA | |
| C. | 2.8g乙烯和丙烯的混合气体中所含碳原子为0.2NA | |
| D. | 1mol苯乙烯中含有的碳碳双键数为4NA |
9.下列有机反应的方程式书写错误的是( )
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. | CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH | ||
| C. | 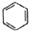 +HNO3$→_{50-60℃}^{浓硫酸}$ +HNO3$→_{50-60℃}^{浓硫酸}$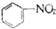 +H2O +H2O | D. | nCH2=CH2$\stackrel{一定条件}{→}$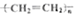 |
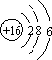 ;羰基硫分子的电子式为
;羰基硫分子的电子式为 .
.