题目内容
1.下列推断不正确的是( )| A. | 稳定性:HF>HCl>HBr>HI | B. | 氧化性:I2>Br2>Cl2 | ||
| C. | 沸点:H2O>NH3 | D. | 还原性:HI>HBr>HCl>HF |
分析 A.根据非金属性的递变规律判断;
B、元素的非金属性越强对应单质的氧化性越强;
C、根据范德华力对物质性质的影响结合H2O、NH3中含有氢键分析;
D、根据同主族元素的非金属性越强,对应的氢化物的还原性越弱.
解答 解:A.F、C1、Br、I的非金属性逐渐减弱,对应的氢化物的稳定性逐渐减弱,故A正确;
B、元素的非金属性越强对应单质的氧化性越强,而元素的非金属性Cl>Br>I,所以单质的氧化性I2<Br2<Cl2,故B错误;
C、组成和结构相似的分子,相对分子质量越大,分子间作用力越强,物质的熔沸点越高,H2O、NH3属于分子晶体,但H2O、NH3中都含有氢键,使得沸点变大,每个H2O中含有2个氢键,每个NH3中含有1个氢键,所以氢化物的沸点:H2O>NH3,故C正确;
D、非金属性:Cl>Br>I,同主族元素的非金属性越强,对应的氢化物的还原性越弱,还原性:HI>HBr>HCl,故D正确;
故选B.
点评 本题考查元素周期律的递变规律,题目难度不大,本题注意C项的判断角度,为易错点.

练习册系列答案
相关题目
11.将2.4g镁和铝的混合物粉末溶于75mL 4mol/L的盐酸中,反应一段时间后,再加入250mL 1.5mol/L的NaOH溶液后待反应完全,此时溶液中大量存在的是( )
| A. | Na+、Mg2+ | B. | Na+、Al3+、Mg2+ | C. | Na+、Mg2+、[Al(OH)4]- | D. | Na+、[Al(OH)4]- |
12.日常用牙膏的主要成分有:活性物质,摩擦剂,甘油等,假设牙膏中的摩擦剂成分为CaC03、SiO2、Al(OH)3中的一种或几种物质组成,牙膏中其他成分均可溶于盐酸,且无气体产生.
(1)牙膏中添加甘油主要作用保温
为进一步炭疽牙膏中摩擦剂成分,进行了以下探究:
Ⅰ.摩擦剂成分的定性检验:
设计实验方案,验证假设,请写出实验步骤以及预期现象和结论(可不填满也可补充).可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水.
Ⅱ.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数

依据实验过程回答下列问题
(2)实验过程中需持续缓缓通入空气,其主要作用将生成的二氧化碳全部排入C中,使之完全被氢氧化钡吸收
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:①氢氧化钡的溶解度大,可以配制得较高的浓度②产物碳酸钡的相对分子量大,可以减小实验误差
(4)下列各项措施中,能提高测定准确经度的是ab(填标号)
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取1.00g样品三份,进行三次测定,测得BaCO2平均质量为3.94g,测样品中碳酸钙的质量分数为20%,若改测定C中生成BaCO2的质量分数,两方法测定的结果不同(填“相同”或“不同”),原因是B中的水蒸气、氯化氢气体等进入装置C中.
(1)牙膏中添加甘油主要作用保温
为进一步炭疽牙膏中摩擦剂成分,进行了以下探究:
Ⅰ.摩擦剂成分的定性检验:
设计实验方案,验证假设,请写出实验步骤以及预期现象和结论(可不填满也可补充).可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水充分搅拌、过滤 | 有难溶物存在 |
| 步骤2: | ①有无色气泡产生,说明有CaCO3 ②出现无色气泡,说明含有碳酸钙,说明有若有难溶物存在,说明有二氧化硅 |
| 步骤3: | |
| … |
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数

依据实验过程回答下列问题
(2)实验过程中需持续缓缓通入空气,其主要作用将生成的二氧化碳全部排入C中,使之完全被氢氧化钡吸收
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:①氢氧化钡的溶解度大,可以配制得较高的浓度②产物碳酸钡的相对分子量大,可以减小实验误差
(4)下列各项措施中,能提高测定准确经度的是ab(填标号)
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取1.00g样品三份,进行三次测定,测得BaCO2平均质量为3.94g,测样品中碳酸钙的质量分数为20%,若改测定C中生成BaCO2的质量分数,两方法测定的结果不同(填“相同”或“不同”),原因是B中的水蒸气、氯化氢气体等进入装置C中.
9.关于下列各图的叙述,正确的是( )
| A. | 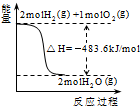 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ•mol-1 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ•mol-1 | |
| B. | 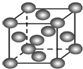 表示Cu形成金属晶体时的堆积方式 表示Cu形成金属晶体时的堆积方式 | |
| C. | 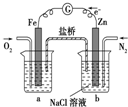 装置中烧杯a中的溶液pH降低 装置中烧杯a中的溶液pH降低 | |
| D. |  装置中待镀铁制品应与电源正极相连 装置中待镀铁制品应与电源正极相连 |
6.下列分子中,所有原子都满足最外层8电子结构且为非极性分子的是( )
| A. | PCl5 | B. | SiH4 | C. | NF3 | D. | CO2 |
13.已知:
分析上表中四种物质的相关数据,请回答:
(1)CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3.
(2)CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是元素的非金属性越强,其氢化物的稳定性越强,分解温度越高.
结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时HCl先液化.
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
(1)CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3.
(2)CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是元素的非金属性越强,其氢化物的稳定性越强,分解温度越高.
结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时HCl先液化.
10.某同学感冒发烧,他可服用下列哪种药品进行治疗( )
| A. | 麻黄碱 | B. | 阿司匹林 | C. | 抗酸药 |
17. 控制适合的条件,将反应AsO43-+2I-+2H+? AsO33-+I2+H2O 设计成如图所示的原电池.下列判断正确的是( )
控制适合的条件,将反应AsO43-+2I-+2H+? AsO33-+I2+H2O 设计成如图所示的原电池.下列判断正确的是( )
 控制适合的条件,将反应AsO43-+2I-+2H+? AsO33-+I2+H2O 设计成如图所示的原电池.下列判断正确的是( )
控制适合的条件,将反应AsO43-+2I-+2H+? AsO33-+I2+H2O 设计成如图所示的原电池.下列判断正确的是( )| A. | 反应开始时,B池中石墨电极上发生氧化反应 | |
| B. | 反应开始时,A池中石墨电极上I-被还原 | |
| C. | 反应开始时,盐桥中K+由左向右迁移 | |
| D. | 电流计读数为零后,在B池中溶入Na3AsO3固体,B池中的石墨电极为正极 |
 A、B、C为短周期元素,在周期表中所处的位置如右图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B的最外层电子数是其电子层数两倍.
A、B、C为短周期元素,在周期表中所处的位置如右图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B的最外层电子数是其电子层数两倍. .
. .
.