题目内容
17.已知有:H、C、O、S、Cl、Fe六种元素,则回答下列有关其性质:(1)Fe原子价电子的排布为3d44s2;Cl位于周期表中位置:第三周期第VIIA族;C原子核外有3个能级.
(2)用“>”或“<”填空:
还原性:HCl<H2S 半径:C>O
(3)在NaOH溶液中用Fe作阳极,通过电解制取FeO42-的电极反应式为:Fe+8OH--6e-═FeO42-+4H2O.
(4)已知1molS完全燃烧生成SO2放出akJ热量;又知2SO3(g)═2SO2(g)+O2(g);△H=bkJ/mol;则请写出1mol固体S生成气体SO3的热化学方程式为S(s)+$\frac{3}{2}$O2(g)=SO3(g)△H=(-a-$\frac{1}{2}$b)kJ•mol-1.
分析 (1)Fe为26号元素,Cl为17号元素,C为6号元素,据此解答即可;
(2)元素的非金属性越强,其氢化物的还原性越弱,同一周期原子序数越大,半径越小;
(3)阳极失去电子,发生氧化反应,化合价升高,据此解答即可;
(4)利用盖斯定律进行计算即可.
解答 解:(1)Fe为26号元素,除以第四周期第VIII族,价电子排布为:3d44s2,Cl处于第三周期第VIIA族,C原子序数为6,有3个能级,分别是1s、2s和2p,故答案为:3d44s2;第三周期第VIIA族;3;
(2)Cl与S处于同一周期,原子序数越大,非金属性越大,氢化物还原性越弱,故还原性:HCl<H2S,原子序数O>C,故半径C>O,故答案为:<;>;
(3)用电化学法制取Na2FeO4,由图可知Fe为阳极失去电子,则阳极反应为Fe+8OH--6e-═FeO42-+4H2O,故答案为:Fe+8OH--6e-═FeO42-+4H2O;(4)已知①S(s)+O2(g)=SO2(g)△H1=-a kJ•mol-1,②SO2(g)+$\frac{1}{2}$O2(g)=SO3(g)△H2=-$\frac{9}{2}$$\frac{1}{2}$bkJ•mol-1;
则利用盖斯定律将①+②可得S(s)+$\frac{3}{2}$O2(g)=SO3(g)△H3=(△H1+△H2)=(-a-$\frac{1}{2}$b)kJ•mol-1,故答案为:S(s)+$\frac{3}{2}$O2(g)=SO3(g)△H=(-a-$\frac{1}{2}$b)kJ•mol-1.
点评 本题综合考查反应热与焓变,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意催化剂对反应的影响以及盖斯定律的应用.

练习册系列答案
相关题目
7.根据中学化学教材所附元素周期表及元素周期律判断,下列叙述正确的是( )
| A. | 在过渡元素中寻找半导体材料 | |
| B. | 元素周期表中第一列元素都是碱金属元素 | |
| C. | 现行元素周期表是按照元素相对原子质量又小到大的顺序排列 | |
| D. | M层电子为奇数的所有主族元素的族序数与该元素原子的M层电子数相等 |
5.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LSO3含有NA个分子 | |
| B. | 标准状况下,22.4LCO2与CO的混合气体含NA个分子 | |
| C. | lmolNa2O2与足量CO2反应转移的电子数为2NA | |
| D. | 常温下NA个H2分子的质量约为2g,它所占的体积约为22.4L |
12.下列有关0.2mol•L-1 BaCl2溶液的说法正确的是( )
| A. | 1L溶液中Cl-离子浓度为0.2mol•L-1 | |
| B. | 1L溶液中Ba2+离子浓度为0.2mol•L-1 | |
| C. | 1L溶液中Cl-离子总数为0.2NA | |
| D. | 1L溶液中Ba2+和Cl-离子总数为0.6NA |
2.在下列各组物质中,属于同系物的是( )
| A. | 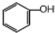 和 和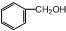 | B. | 丙烷和2,2一二甲基丙烷 | ||
| C. | 乙二醇和丙三醇 | D. | 1,1一二氯乙烷和1,2一二氯乙烷 |
9.用如图所示装置电解CuCl2溶液,下列判断正确的是( )
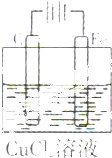

| A. | C棒是阴极 | B. | Cu2+向C棒电极移动 | ||
| C. | Fe电极发生还原反应 | D. | 溶液颜色逐渐加深 |
7.下列关于物质分类或归类正确的是( )
| A. | 化合物:CaCl2、NaOH、HCl、HD | B. | 同系物:苯、甲苯、乙苯 | ||
| C. | 有机物:橡胶、硅胶、纤维素、乙醇 | D. | 官能团:氯离子、羟基、硝基、苯 |