题目内容
9.如图所示装置适用于实验室制氨气并验证氨气的某化学性质,其中能达到实验目的是( )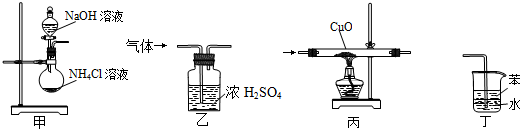
| A. | 用装置甲制取氨气 | B. | 用装置乙除去氨气中的水蒸气 | ||
| C. | 用装置丙验证氨气具有还原性 | D. | 用装置丁吸收氨气 |
分析 A.氨气易溶于水,易挥发,应加热;
B.氨气和浓硫酸反应;
C.加热条件下,氨气与氧化铜发生氧化还原反应;
D.氨气直接通入水中,不能防止倒吸.
解答 解:A.氨气易溶于水,易挥发,应用浓氢氧化钠溶液和氯化铵反应,且加热,故A错误;
B.氨气和浓硫酸反应,应用碱石灰干燥氨气,故B错误;
C.加热条件下,氨气与氧化铜发生氧化还原反应,根据氧化铜的颜色变化可判断是否发生氧化还原反应,故C正确;
D.氨气直接通入水中,不能防止倒吸,应用四氯化碳,故D错误.
故选C.
点评 本题考查化学实验方案的评价,侧重于学生对基本实验操作正确与否的判断的考查,要求同学们要熟练掌握物质的基本物理和化学性质,注意基本实验操作的要领和实验要求.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
19.X、Y、Z、W、R均为第三周期主族元素,且原子序数依次增大.X、Y、W的最高价氧化物对应水化物两两之间都能发生反应,Z的单质具有半导体的特性,W原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | X与氧元素形成的化合物中可能含有共价键 | |
| B. | 第三周期元素的简单离子中Y离子的半径最小 | |
| C. | Z、W的氧化物均为酸性氧化物 | |
| D. | R元素含氧酸的酸性一定强于W |
17.亚硝酸钠(NaNO2)是一种常用的防腐剂,有咸味,易溶于水,有毒.在320℃时分解生成有刺激性气味的气体,与盐酸作用会放出红棕色气体.亚硝酸钠在食品中的添加量必须严格控制.下列说法不正确的是( )
| A. | 可用盐酸鉴别亚硝酸钠和食盐 | |
| B. | 亚硝酸钠可以加到食品中,但添加量要符合规定 | |
| C. | 亚硝酸钠受热分解放出的气体可能是NH3 | |
| D. | 亚硝酸钠由三种元素组成 |
1.室温下,在10mL0.1mol/LNH4Al(SO4)2溶液中,下列说法正确的是( )
| A. | 水电离出的c(H+)>10-7mol/L | |
| B. | c(Al3+)=c(NH4+)+c(NH3•H2O) | |
| C. | Ca2+、HCO3-、Na+、Cl-能在该溶液中大量共存 | |
| D. | 向该溶液中滴加10mL0.1mol/L NaOH溶液,无沉淀生成 |
18.化学与科技、生产、生活密切相关.下列说法正确的是( )
| A. | 气象环境报告中的“PM2.5”是一种新分子的描述 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量、 | |
| C. | “玉兔号”月球车太阳能电池帆板的材料是二氧化硅 | |
| D. | 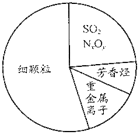 如图为雾霾的主要成分示意图,SO2和NxOy都属于酸性氧化物 |
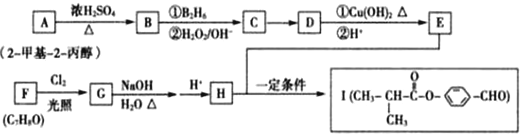
 .
.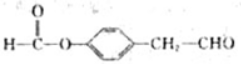 、
、 .
.