题目内容
【题目】某试剂瓶上贴有如下标签,对该试剂理解正确的是
![]()
A. 该溶液中含有的微粒主要有:NaCl、Na+、Cl-、H2O
B. 若取50毫升溶液,其中的c(Cl-)=0.05 mol/L
C. 若取该溶液与0.1 mol/L AgNO3 100 mL溶液完全反应,需要取该溶液10 mL
D. 该溶液与1.0mol/LNa2SO4溶液的c(Na+)相等
【答案】C
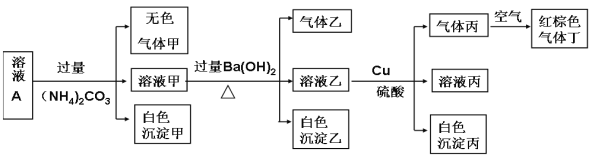
【解析】A. 氯化钠溶于水全部电离出Na+、Cl-,溶液中不存在NaCl,A错误;B. 溶液是均一稳定的,若取50毫升溶液,其中c(Cl-)=1.0mol/L,B错误;C. 100 mL 0.1 mol/L AgNO3溶液中硝酸银的物质的量是0.01mol,完全反应消耗氯化钠是0.01mol,因此需要取该溶液的体积为0.01mol÷1mol/L=0.01L=10 mL,C正确;D. 该溶液与1.0mol/LNa2SO4溶液的c(Na+)不相等,后者溶液中钠离子浓度是2.0mol/L,D错误,答案选C。

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
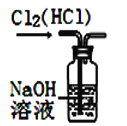
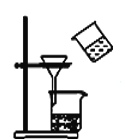
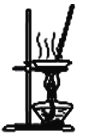
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
|
|
A.用CCl4提取溴水中的Br2 | B.从KI和I2的固体混合物中回收I2 |
|
|
C.稀释浓硫酸 | D.工业酒精制备无水酒精 |
A. A B. B C. C D. D