题目内容
【题目】下列反应中,氧化剂与还原剂的物质的量之比为1:2的是
①2CH3COOH+Ca(C1O)2=2HC1O+Ca(CH3COO)2
② SiO2+2C![]() Si+2CO↑
Si+2CO↑
③4HC1(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
④SiO2+3C![]() SiC+2CO↑
SiC+2CO↑
A. 仅有② B. 仅有②④ C. 仅有②③④ D. ①②③④
【答案】C
【解析】
①反应中没有元素化合价的变化,不是氧化还原反应,①不符合题意;
②中硅元素的化合价降低,碳元素的化合价升高,则SiO2为氧化剂,C为还原剂,其物质的量之比为1:2,①符合题意;
③HCl为还原剂,MnO2为氧化剂,且4molHCl反应时只有2mol作还原剂,根据反应过程中原子守恒可知,氧化剂与还原剂的物质的量之比为1:2,③符合题意;
④只有C元素的化合价变化,C为还原剂、氧化剂,根据反应过程原子守恒、电子守恒可知,氧化剂与还原剂的物质的量之比为1:2,④符合题意,符合题意的是②③④;
故正确选项为C。

【题目】在下右图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b不满足题目要求的是
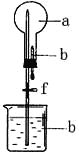
选项 | a(干燥气体) | b(液体) |
A | Cl2 | 饱和NaOH溶液 |
B | SO2 | 4mol/LNaOH溶液 |
C | NO2 | 水 |
D | NH3 | 1mol/L盐酸 |
A. A B. B C. C D. D
【题目】在四个恒容密闭容器中按左下表相应量充入气体,发生反应2N2O(g)![]() 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如下图所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如下图所示:
容器 | 容积/L | 起始物质的量/mol | ||
N2O | N2 | O2 | ||
Ⅰ | V1 | 0.1 | 0 | 0 |
Ⅱ | 1.0 | 0.1 | 0 | 0 |
Ⅲ | V3 | 0.1 | 0 | 0 |
Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 |
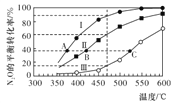
下列说法正确的是
A. 该反应的正反应放热
B. 相同温度下反应相同时间,平均反应速率:v(Ⅰ)>v(Ⅱ)
C. 容器Ⅳ在470℃进行反应时,起始反应速率:v正(N2O)<v逆(N2O)
D. 图中A、B、C三点处容器内总压强:pA(I)< pB(Ⅱ)<pC(Ⅲ)